बेंजीन की संरचना। "सुगंधित हाइड्रोकार्बन (एरेन्स)
बेंजीन की संरचना पर आधुनिक दृष्टिकोण: एक सपाट अणु, जिसके कार्बन परमाणु एसपी 2 संकरण की स्थिति में होते हैं और एक नियमित षट्भुज में संयुक्त होते हैं।

एक बेंजीन अणु का चित्र:
![]()
सुगंध- -इलेक्ट्रॉनों के निरूपण के कारण अप्रकाशित अवस्था की असामान्य रूप से कम ऊर्जा।
सुगंध- एक अवधारणा जो संयुग्मित बंधनों की एक प्रणाली के साथ चक्रीय संरचनाओं की प्रतिक्रियाशीलता की संरचनात्मक, ऊर्जा गुणों और विशेषताओं की समग्रता को दर्शाती है
सुगंध के लक्षणकोई भी यौगिक सुगंधित होता है यदि इसमें: क) एक सपाट बंद चक्र; बी) संयुग्मित π-इलेक्ट्रॉन प्रणाली चक्र के सभी परमाणुओं को कवर करती है; ग) यदि संयुग्मन में शामिल इलेक्ट्रॉनों की संख्या हकल सूत्र (4n + 2., जहां n चक्रों की संख्या है) से मेल खाती है।
संवयविता

नामपद्धति

ऑर्थो-, मेटाऔर जोड़ा-प्रतिस्थापित:


भौतिक गुण
सभी सुगंधित यौगिकों में एक गंध होती है। बेंजीन, टोल्यूनि, जाइलीन, एथिलबेन्जीन,
कमीन, स्टाइरीन - तरल पदार्थ, नेफ़थलीन, एन्थ्रेसीन - ठोस।
26. बेंजीन श्रृंखला के सुगंधित हाइड्रोकार्बन। नामपद्धति। समरूपता। बेंजीन और उसके होमोलॉग प्राप्त करने के तरीके: कोल टार से, पैराफिन के एरोमेटाइजेशन और डीहाइड्रोसाइक्लाइज़ेशन, वर्टज़-फिटिग प्रतिक्रिया के अनुसार, ओलेफ़िन के साथ फ्राइडल-क्राफ्ट्स अल्काइलेशन, बेंजोइक एसिड के लवण से एल्काइल, अल्कोहल, अल्काइन का ट्रिमराइज़ेशन।
एरेन्स (सुगंधित हाइड्रोकार्बन) चक्रीय यौगिक होते हैं जिनके अणुओं में एक या अधिक बेंजीन नाभिक होते हैं। बेंजीन का अनुभवजन्य सूत्र C6H6
संवयविता
डी-, ट्राई- और टेट्रासबस्टिट्यूटेड एरोमैटिक हाइड्रोकार्बन के लिए, प्रतिस्थापक की स्थिति का आइसोमेरिज्म और साइड एल्काइल चेन का आइसोमेरिज्म विशेषता है।

मोनो-, पेंटा- और हेक्सा-प्रतिस्थापित एरेन में रिंग में प्रतिस्थापक की स्थिति से जुड़े आइसोमर्स नहीं होते हैं।
नामपद्धति
बेंजीन डेरिवेटिव को प्रतिस्थापित बेंजीन कहा जाता है। उनमें से कई के लिए, या तो तुच्छ नामों का उपयोग किया जाता है, या "बेंजीन" शब्द से पहले एक उपसर्ग द्वारा प्रतिस्थापित किया जाता है। मोनोसबस्टिट्यूटेड बेंजीन के मामले में, नामों में संख्याएं शामिल नहीं हैं, क्योंकि बेंजीन अणु के सभी छह कार्बन परमाणु समतुल्य हैं, प्रत्येक प्रतिस्थापक के लिए केवल एक मोनोसबस्टिट्यूटेड बेंजीन संभव है।

यदि बेंजीन अणु में दो प्रतिस्थापन हैं, तो तीन अलग-अलग अप्रतिस्थापित बेंजीन हो सकते हैं। उनके अनुसार नाम दिया गया है ऑर्थो-, मेटाऔर जोड़ा-प्रतिस्थापित:

यदि बेंजीन में तीन या अधिक प्रतिस्थापन हैं, तो रिंग में उनकी स्थिति केवल संख्याओं द्वारा इंगित की जानी चाहिए। सभी मामलों में, स्थानापन्नों के नाम "बेंजीन" शब्द से पहले वर्णानुक्रम में सूचीबद्ध हैं। नाम में नंबर 1 छोड़ा जा सकता है, जिस विकल्प से उलटी गिनती शुरू होती है, इस मामले में नाम के आधार पर शामिल किया गया है:

रसीद:
1. कोलतार प्रसंस्करण, तेल आसवन, शुष्क आसवन
लकड़ी।
2. तेल का सुगंधितकरण।

3. हेक्सेन और हेप्टेन का निर्जलीकरण।
सी 6 एच 14 → सी 6 एच 6 + 4 एच 2
सी 7 एच 16 → सी6एच5-सीएच3 + 4एच2
4. वर्ट्ज़-फिटिग:

फ्राइडल-शिल्प के अनुसार क्षारीकरण। प्रतिक्रिया के लिए दो संभावित तंत्र स्वीकार किए जाते हैं। पहले मामले में, इलेक्ट्रोफिलिक कण एक कार्बोकेशन है जो एल्यूमीनियम क्लोराइड (लुईस एसिड) के साथ एक हेलोकेन की बातचीत के परिणामस्वरूप बनता है:
दूसरे मामले में, यह माना जा सकता है कि एल्काइल हैलाइड के साथ AlCl3 के ध्रुवीय परिसर का एल्काइल समूह इलेक्ट्रोफाइल के रूप में कार्य करता है।
बेंजीन का क्षारीकरण (फ्रीडल-शिल्प प्रतिक्रिया)
सी 6 एच 6 + सी 2 एच 5 सीएल → सी 6 एच 5-सी 2 एच 5 + एचसीएल
27सुगंधित श्रृंखला में इलेक्ट्रोफिलिक प्रतिस्थापन (नाइट्रेशन, सल्फोनेशन, हैलोजनेशन, एल्केलेशन और फ्रीडेल-क्राफ्ट्स एसाइलेशन)। - और -परिसरों की अवधारणा। इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं का तंत्र
प्रतिक्रियाओं का पहला समूह प्रतिस्थापन प्रतिक्रियाएं हैं। हमने कहा कि आण्विक संरचना में एरेन्स के कई बंधन नहीं होते हैं, लेकिन इसमें छह इलेक्ट्रॉनों की एक संयुग्मित प्रणाली होती है, जो बहुत स्थिर होती है और बेंजीन की अंगूठी को अतिरिक्त ताकत देती है। इसलिए, रासायनिक प्रतिक्रियाओं में, सबसे पहले, हाइड्रोजन परमाणुओं का प्रतिस्थापन होता है, न कि बेंजीन की अंगूठी का विनाश।
अल्केन्स के बारे में बात करते समय हम पहले ही प्रतिस्थापन प्रतिक्रियाओं का सामना कर चुके हैं, लेकिन उनके लिए ये प्रतिक्रियाएं एक कट्टरपंथी तंत्र के अनुसार आगे बढ़ीं, जबकि एरेन्स को प्रतिस्थापन प्रतिक्रियाओं के एक आयनिक तंत्र की विशेषता है।
प्रथमरासायनिक गुण - हलोजन। हैलोजन परमाणु के लिए हाइड्रोजन परमाणु का प्रतिस्थापन - क्लोरीन या ब्रोमीन।
गर्म होने पर और हमेशा उत्प्रेरक की भागीदारी के साथ प्रतिक्रिया आगे बढ़ती है। क्लोरीन के मामले में, यह एल्यूमीनियम क्लोराइड या आयरन क्लोराइड तीन हो सकता है। उत्प्रेरक हलोजन अणु का ध्रुवीकरण करता है, जिसके परिणामस्वरूप हेटेरोलाइटिक बंधन टूट जाता है और आयन प्राप्त होते हैं।
धनावेशित क्लोराइड आयन बेंजीन के साथ अभिक्रिया करता है।
यदि ब्रोमीन के साथ अभिक्रिया होती है, तो आयरन ट्राइब्रोमाइड या एल्युमिनियम ब्रोमाइड उत्प्रेरक का कार्य करता है।

यह ध्यान रखना महत्वपूर्ण है कि प्रतिक्रिया आणविक ब्रोमीन के साथ होती है न कि ब्रोमीन पानी के साथ। बेंजीन ब्रोमीन के पानी के साथ प्रतिक्रिया नहीं करता है।
बेंजीन होमोलॉग के हलोजन की अपनी विशेषताएं हैं। टोल्यूनि अणु में, मिथाइल समूह रिंग में प्रतिस्थापन की सुविधा देता है, प्रतिक्रियाशीलता बढ़ जाती है, और प्रतिक्रिया मामूली परिस्थितियों में होती है, यानी पहले से ही कमरे के तापमान पर।
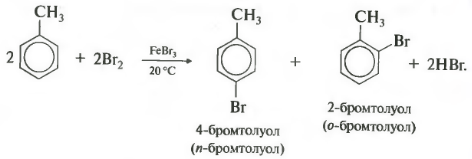
यह ध्यान रखना महत्वपूर्ण है कि प्रतिस्थापन हमेशा ऑर्थो और पैरा स्थितियों में होता है, इसलिए आइसोमर्स का मिश्रण प्राप्त होता है।
दूसरासंपत्ति - बेंजीन का नाइट्रेशन, बेंजीन रिंग में नाइट्रो समूह की शुरूआत।
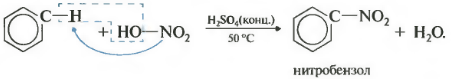
कड़वे बादाम की गंध के साथ एक भारी पीला तरल बनता है - नाइट्रोबेंजीन, इसलिए बेंजीन के लिए प्रतिक्रिया गुणात्मक हो सकती है। नाइट्रेशन के लिए, सांद्र नाइट्रिक और सल्फ्यूरिक एसिड के नाइट्रेटिंग मिश्रण का उपयोग किया जाता है। अभिक्रिया गर्म करके की जाती है।
आपको याद दिला दूं कि कोनोवलोव प्रतिक्रिया में अल्केन्स के नाइट्रेशन के लिए सल्फ्यूरिक एसिड को मिलाए बिना तनु नाइट्रिक एसिड का उपयोग किया गया था।
टोल्यूनि के नाइट्रेशन में, साथ ही हैलोजन में, ऑर्थो- और पैरा-आइसोमर्स का मिश्रण बनता है।
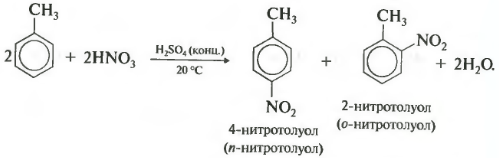
तीसरागुण - बेंजीन का हैलोऐल्केन के साथ क्षारीकरण।

यह प्रतिक्रिया बेंजीन रिंग में एक हाइड्रोकार्बन रेडिकल की शुरूआत की अनुमति देती है और इसे बेंजीन होमोलॉग प्राप्त करने की एक विधि माना जा सकता है। एल्युमिनियम क्लोराइड का उपयोग उत्प्रेरक के रूप में किया जाता है, जो हैलोकेन अणु के आयनों में अपघटन को बढ़ावा देता है। इसे गर्म करने की भी जरूरत है।
चौथीगुण - बेंजीन का एल्कीन के साथ क्षारीकरण।
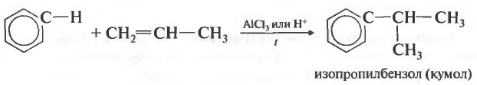
इस तरह, उदाहरण के लिए, कमीन या एथिलबेन्जीन प्राप्त किया जा सकता है। उत्प्रेरक एल्यूमीनियम क्लोराइड है।
2. बेंजीन के अलावा की प्रतिक्रियाएं
प्रतिक्रियाओं का दूसरा समूह जोड़ प्रतिक्रियाएं हैं। हमने कहा कि ये प्रतिक्रियाएं विशेषता नहीं हैं, लेकिन वे पाई-इलेक्ट्रॉन बादल के विनाश और छह सिग्मा बांडों के गठन के साथ कठोर परिस्थितियों में संभव हैं।
पांचवांसामान्य सूची में संपत्ति - हाइड्रोजनीकरण, हाइड्रोजन का जोड़।
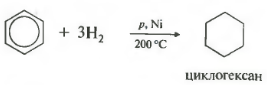
तापमान, दबाव, उत्प्रेरक निकल या प्लैटिनम। टोल्यूनि उसी तरह प्रतिक्रिया करने में सक्षम है।
छठासंपत्ति - क्लोरीनीकरण। कृपया ध्यान दें कि हम विशेष रूप से क्लोरीन के साथ बातचीत के बारे में बात कर रहे हैं, क्योंकि ब्रोमीन इस प्रतिक्रिया में प्रवेश नहीं करता है।
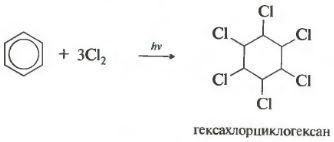
प्रतिक्रिया कठोर पराबैंगनी विकिरण के तहत आगे बढ़ती है। हेक्साक्लोरोसायक्लोहेक्सेन, हेक्साक्लोरेन का दूसरा नाम, बनता है, एक ठोस।
यह याद रखना महत्वपूर्ण है कि बेंजीन के लिए संभव नहींहाइड्रोजन हैलाइड्स (हाइड्रोहैलोजनेशन) और पानी (हाइड्रेशन) की जोड़ प्रतिक्रियाएँ।
3. बेंजीन होमोलॉग्स की साइड चेन में प्रतिस्थापन
प्रतिक्रियाओं का तीसरा समूह केवल बेंजीन होमोलॉग्स की चिंता करता है - यह साइड चेन में एक प्रतिस्थापन है।
सातवींसामान्य सूची में एक संपत्ति पार्श्व श्रृंखला में अल्फा कार्बन परमाणु पर हलोजन है।

प्रतिक्रिया तब होती है जब गर्म या विकिरणित होता है, और हमेशा केवल अल्फा कार्बन पर। जैसे ही हलोजन जारी रहता है, दूसरा हलोजन परमाणु अल्फा स्थिति में वापस आ जाएगा।
4. बेंजीन समरूपों का ऑक्सीकरण
प्रतिक्रियाओं का चौथा समूह ऑक्सीकरण है।
बेंजीन की अंगूठी बहुत मजबूत है, इसलिए बेंजीन ऑक्सीकरण नहीं करता हैपोटैशियम परमैंगनेट - इसके विलयन का रंग नहीं बदलता है। यह याद रखना बहुत जरूरी है।
दूसरी ओर, बेंजीन समरूपों को गर्म करने पर पोटेशियम परमैंगनेट के अम्लीकृत घोल से ऑक्सीकृत किया जाता है। और यह आठवां रासायनिक गुण है।

यह बेंजोइक एसिड निकलता है। समाधान का मलिनकिरण मनाया जाता है। इस मामले में, प्रतिस्थापक की कार्बन श्रृंखला कितनी भी लंबी क्यों न हो, यह हमेशा पहले कार्बन परमाणु के बाद टूट जाती है और अल्फा परमाणु बेंजोइक एसिड के गठन के साथ एक कार्बोक्सिल समूह में ऑक्सीकृत हो जाता है। शेष अणु संबंधित एसिड में ऑक्सीकृत हो जाता है या, यदि यह केवल एक कार्बन परमाणु है, तो कार्बन डाइऑक्साइड में।
यदि बेंजीन होमोलॉग में सुगंधित वलय पर एक से अधिक हाइड्रोकार्बन पदार्थ होते हैं, तो ऑक्सीकरण समान नियमों के अनुसार होता है - अल्फा स्थिति में कार्बन ऑक्सीकृत होता है।
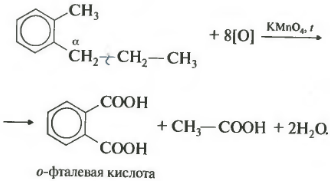
इस उदाहरण में, एक द्विक्षारकीय ऐरोमैटिक अम्ल प्राप्त होता है, जिसे phthalic अम्ल कहा जाता है।
एक विशेष तरीके से, मैं सल्फ्यूरिक एसिड की उपस्थिति में वायुमंडलीय ऑक्सीजन के साथ, क्यूमिन, आइसोप्रोपिलबेन्जीन के ऑक्सीकरण को नोट करता हूं।
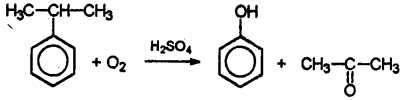
यह फिनोल के उत्पादन के लिए तथाकथित कमीन विधि है। एक नियम के रूप में, फिनोल के उत्पादन से संबंधित मामलों में इस प्रतिक्रिया से निपटना पड़ता है। यह औद्योगिक तरीका है।
नौवांगुण - दहन, ऑक्सीजन के साथ पूर्ण ऑक्सीकरण। बेंजीन और उसके समरूप कार्बन डाइऑक्साइड और पानी को जलाते हैं।
आइए हम बेंजीन के दहन के समीकरण को सामान्य रूप में लिखें।
द्रव्यमान के संरक्षण के नियम के अनुसार, बाईं ओर उतने ही परमाणु होने चाहिए जितने दाईं ओर परमाणु हैं। क्योंकि रासायनिक प्रतिक्रियाओं में परमाणु कहीं नहीं जाते, लेकिन उनके बीच बंधनों का क्रम बस बदल जाता है। तो उतने ही कार्बन डाइऑक्साइड अणु होंगे जितने कि एक एरीन अणु में कार्बन परमाणु होते हैं, क्योंकि अणु में एक कार्बन परमाणु होता है। वह एन सीओ 2 अणु है। हाइड्रोजन परमाणुओं की तुलना में आधे पानी के अणु होंगे, यानी (2n-6) / 2, जिसका अर्थ है n-3।
बाईं ओर और दाईं ओर समान संख्या में ऑक्सीजन परमाणु होते हैं। दाईं ओर, कार्बन डाइऑक्साइड से 2n हैं, क्योंकि प्रत्येक अणु में दो ऑक्सीजन परमाणु होते हैं, साथ ही पानी से n-3, कुल 3n-3 के लिए। बाईं ओर, ऑक्सीजन परमाणुओं की संख्या समान है - 3n-3, जिसका अर्थ है कि आधे अणु हैं, क्योंकि अणु में दो परमाणु होते हैं। यानी (3n-3)/2 ऑक्सीजन अणु।
इस प्रकार, हमने सामान्य रूप में बेंजीन होमोलॉग के दहन के लिए समीकरण संकलित किया है।
रासायनिक संरचना
बेंजीन अणु में कार्बन परमाणु एक नियमित सपाट षट्भुज बनाते हैं, हालांकि इसे आमतौर पर लम्बा खींचा जाता है।
बेंजीन अणु की संरचना अंततः एसिटिलीन से इसके गठन की प्रतिक्रिया से पुष्टि की गई थी। संरचनात्मक सूत्र तीन सिंगल और तीन डबल अल्टरनेटिंग कार्बन-कार्बन बॉन्ड दिखाता है। लेकिन ऐसी छवि अणु की वास्तविक संरचना को व्यक्त नहीं करती है। वास्तव में, बेंजीन में कार्बन-कार्बन बांड समतुल्य होते हैं, और उनके पास ऐसे गुण होते हैं जो एकल या दोहरे बंधनों के समान नहीं होते हैं। इन विशेषताओं को बेंजीन अणु की इलेक्ट्रॉनिक संरचना द्वारा समझाया गया है।
बेंजीन की इलेक्ट्रॉनिक संरचना
बेंजीन अणु में प्रत्येक कार्बन परमाणु sp 2 संकरण की अवस्था में होता है। यह दो आसन्न कार्बन परमाणुओं और एक हाइड्रोजन परमाणु से तीन y-बंधों से जुड़ा होता है। नतीजतन, एक सपाट षट्भुज बनता है: सभी छह कार्बन परमाणु और सभी C--C और C-H y-बंध एक ही तल में स्थित होते हैं। चौथे इलेक्ट्रॉन (पी-इलेक्ट्रॉन) के इलेक्ट्रॉन बादल, जो संकरण में शामिल नहीं है, में डंबल का आकार होता है और बेंजीन रिंग के विमान के लंबवत उन्मुख होता है। पड़ोसी कार्बन परमाणुओं के ऐसे पी-इलेक्ट्रॉन बादल वलय के तल के ऊपर और नीचे ओवरलैप करते हैं। नतीजतन, छह पी-इलेक्ट्रॉन सभी कार्बन परमाणुओं के लिए एक सामान्य इलेक्ट्रॉन बादल और एक रासायनिक बंधन बनाते हैं। बड़े इलेक्ट्रॉन तल के दो क्षेत्र y-बंध तल के दोनों ओर स्थित होते हैं।
पी-इलेक्ट्रॉन बादल कार्बन परमाणुओं के बीच की दूरी में कमी का कारण बनता है। बेंजीन अणु में, वे समान और 0.14 एनएम के बराबर होते हैं। सिंगल और डबल बॉन्ड के मामले में, ये दूरियां क्रमशः 0.154 और 0.134 एनएम होंगी। इसका मतलब है कि बेंजीन अणु में कोई एकल और दोहरा बंधन नहीं हैं। बेंजीन अणु एक ही विमान में पड़े समान सीएच-समूहों का एक स्थिर छह-सदस्यीय चक्र है। बेंजीन में कार्बन परमाणुओं के बीच सभी बंधन समतुल्य हैं, जो बेंजीन नाभिक के विशिष्ट गुणों को निर्धारित करता है। यह बेंजीन के संरचनात्मक सूत्र द्वारा एक नियमित षट्भुज के रूप में (I) के अंदर एक चक्र के साथ सबसे सटीक रूप से परिलक्षित होता है। (चक्र कार्बन परमाणुओं के बीच बंधों की समानता का प्रतीक है।) हालांकि, केकुले सूत्र का उपयोग अक्सर किया जाता है, जो दोहरे बंधन (II) को दर्शाता है।
पाठ प्रकार:नई सामग्री सीखने का पाठ।
सबक का प्रकार:समस्या व्याख्यान।
पाठ का मुख्य उपदेशात्मक लक्ष्य:सभी छात्रों द्वारा शैक्षिक सामग्री की सामग्री की समझ हासिल करना।
पाठ के सीखने के उद्देश्य:
- हाइड्रोकार्बन के बारे में गहन ज्ञान;
- छात्रों को एक नए प्रकार के रासायनिक बंधन से परिचित कराने के लिए, बेंजीन के उदाहरण का उपयोग करते हुए, यौगिकों के इस समूह की विशेषता; सुगंधितता की अवधारणा दें;
पाठ के उद्देश्यों का विकास करना:
- छात्रों में शैक्षिक सामग्री में मुख्य, आवश्यक, तुलना, सामान्यीकरण और व्यवस्थित करने, कारण और प्रभाव संबंध स्थापित करने की क्षमता विकसित करने के लिए;
- व्यक्ति के स्वैच्छिक और भावनात्मक गुणों के विकास को बढ़ावा देना;
- छात्रों के विषय और भाषण में रुचि के विकास पर विशेष ध्यान दें।
पाठ के शैक्षिक उद्देश्य:विश्वदृष्टि विचारों के निर्माण में योगदान:
- दुनिया की भौतिकता;
- अनुभूति की प्रक्रिया की निरंतरता।
सबक उपकरण:
- अभिकर्मकों: बेंजीन, समाधान KMnO 4 , ब्रोमीन पानी;
- बेंजीन अणु का बॉल-एंड-स्टिक मॉडल (केकुले के अनुसार);
- संदर्भ नोट्स, टेबल।
कक्षाओं के दौरान
पाठ के लिए एपिग्राफ:
"शिक्षा ज्ञान की मात्रा में शामिल नहीं है,
लेकिन सभी की पूरी समझ और कुशल अनुप्रयोग में
तुम क्या जानते हो।"
ए. डिस्टरवेग।
पिछले पाठ में, मैंने किसी पदार्थ का सूत्र खोजने और अध्ययन की गई कक्षाओं के पदार्थों को चिह्नित करने के लिए समस्याओं के समाधान को दोहराने के लिए कहा।
हम किसी पदार्थ के आणविक सूत्र को खोजने के लिए समस्याओं को हल करते हैं और उन पदार्थों का विवरण देते हैं जो प्राप्त संरचना के अनुरूप होते हैं।
ब्लैकबोर्ड के लिए:
1 + 2 छात्र (कार्ड पर समस्याओं को हल करें)।
कार्य 1
82.75% कार्बन 17.25% हाइड्रोजन युक्त पदार्थ का सूत्र व्युत्पन्न कीजिए। वायु में इस पदार्थ का आपेक्षिक वाष्प घनत्व 2 है।
टास्क #2
हाइड्रोकार्बन का आणविक सूत्र निर्धारित करें, कार्बन का द्रव्यमान अंश जिसमें 85.7% है, और हाइड्रोजन - 14.3% है। हाइड्रोजन के सापेक्ष किसी पदार्थ का आपेक्षिक घनत्व 28 है।

ब्लैकबोर्ड पर कक्षा + छात्र:
टास्क #3
किसी पदार्थ का आणविक सूत्र क्या होता है जिसमें कार्बन का द्रव्यमान अंश 93.2% होता है। हाइड्रोजन का आपेक्षिक घनत्व 39 है।
उत्तर: C6H6 सही सूत्र है
तीसरी समस्या को हल करते समय, हमें रचना C6H6 की संख्या मिली। इस पदार्थ को हाइड्रोकार्बन के किस ज्ञात वर्ग के लिए जिम्मेदार ठहराया जा सकता है?
हम इस पदार्थ को हाइड्रोकार्बन के किसी भी अध्ययन वर्ग के लिए जिम्मेदार नहीं ठहरा सकते हैं।
तो, समस्या!, जिसे हमें मिलकर हल करना है। आज हम आइए, ऐरोमैटिक नामक हाइड्रोकार्बन के एक नए समूह से परिचित हों।
पाठ का विषय: सुगंधित हाइड्रोकार्बन (एरेन्स)। बेंजीन। अणु की संरचना।
आज हमारे मुख्य कार्य:
- हाइड्रोकार्बन के बारे में ज्ञान को गहरा करें, कार्बनिक यौगिकों की विविधता की समझ का विस्तार करें।
- एक नए प्रकार के रासायनिक बंधन से परिचित होने के लिए, हाइड्रोकार्बन के इस समूह की विशेषता।
व्याख्यान योजना:
- एरेन्स हाइड्रोकार्बन के वर्गों में से एक हैं।
- बेंजीन की खोज का इतिहास।
- बेंजीन अणु की संरचना।
क) केकुल के अनुसार बेंजीन की संरचना;
बी) बेंजीन की इलेक्ट्रॉनिक संरचना के बारे में आधुनिक विचार;
सी) एक सुगंधित नाभिक और डेढ़ बंधन की अवधारणा।
डी / एस के साथ। 51-53, व्याख्यान का सारांश तैयार करें।
आज के पाठ में हम हाइड्रोकार्बन के एक नए समूह से परिचित होंगे जिसे एरोमेटिक्स या एरेन्स कहा जाता है।
खुशबूदारइन हाइड्रोकार्बनों का नाम इसलिए रखा गया क्योंकि उनमें से पहले ज्ञात प्रतिनिधियों में एक सुखद था महक।बाद में पता चला कि अधिकांश पदार्थ रासायनिक रूप से हैं। गुण एक ही समूह के हैं, कोई सुगंधित गंध नहीं है। हालाँकि, इन यौगिकों का ऐतिहासिक रूप से स्थापित सामान्य नाम आज तक उनके पास बना हुआ है।
सुगंधित हाइड्रोकार्बन का सबसे सरल प्रतिनिधि बेंजीन है।
कारण और प्रभाव संबंधों के आधार पर हाइड्रोकार्बन के पिछले वर्गों का अध्ययन किया गया है: रचना - संरचना - गुण - अनुप्रयोग।हम अभी के लिए उसी तार्किक सिद्धांत को छोड़ देंगे।
मिश्रणपदार्थ हम स्थापना- सी 6 एच 6. यह बेंजीन है। बेंजीन भी एक हाइड्रोकार्बन है, लेकिन एक हाइड्रोकार्बन मूल रूप से चर्चा किए गए लोगों से अलग है। बेंजीन क्या है?
आइए बेंजीन की खोज के इतिहास के बारे में जानें। (छात्र संदेश)।
पहला छात्र।
1825 में, एम। फैराडे ने उस समय इंग्लैंड में कोयले से उत्पादित प्रकाश गैस से अलग किया, एक तरल जिसमें कार्बन और हाइड्रोजन शामिल थे। कुछ साल बाद (1834 में)
बेंजोइक एसिड के आसवन के दौरान, ई। मिचरलिच ने फैराडे के समान एक पदार्थ प्राप्त किया, जिसे बेंजोइक एसिड के साथ आनुवंशिक संबंध पर जोर देने के लिए इसे गैसोलीन कहा जाता है, और पाया कि इसकी मौलिक संरचना सी 6 एच 6 (एंग्लो-सैक्सन में) है। देशों में, यह नाम अभी भी बेंजीन के लिए संरक्षित है)।
बाद में, जे. लिबिग ने इस यौगिक को एक मूल नाम देने की सिफारिश की - बेंजीन (अंत - ओएल लैटिन ओलीम - तेल से इसके तैलीय चरित्र को इंगित करता है)। 1845 में, ए.वी. हॉफमैन ने पहली बार बेंजीन को कोल टार से अलग किया।
दूसरा छात्र।
एक सुगंधित यौगिक के रूप में बेंजीन की संरचना के सिद्धांत का "जन्मदिन" 27 जनवरी, 1865 है - वह दिन जब पेरिस केमिकल सोसाइटी के बुलेटिन में "सुगंधित पदार्थों का संविधान" पर जानकारी प्रकाशित हुई थी।
आइए अगले चरण पर चलते हैं: आइए हम बेंजीन अणु की संरचना स्थापित करें।जैसा कि हम पहले ही निर्धारित कर चुके हैं, बेंजीन को हाइड्रोकार्बन के किसी भी ज्ञात वर्ग के लिए जिम्मेदार नहीं ठहराया जा सकता है। लेकिन, आइए कल्पना करने की कोशिश करें कि इसके सूत्र के कौन से रूप हो सकते हैं:

आप आइसोमर्स के साथ भी आ सकते हैं जो डबल और ट्रिपल बॉन्ड की स्थिति में भिन्न होते हैं।
अब हमारे पास वह है जिसे कहा जाता है कार्य परिकल्पना।आइए इसे जांचने की कोशिश करें। यदि हमारे द्वारा प्रस्तावित संरचनाओं में से किसी एक की शुद्धता को सिद्ध करना संभव है, परिकल्पना सिद्धांत बन जाती हैनहीं तो हम आगे सोचेंगे।
बहुत हैं एक साधारण प्रतिक्रियाकौन सा की अनुमति देता हैजल्दी और मज़बूती से उपलब्धता स्थापित करें डबल या ट्रिपल बॉन्डअसंतृप्त हाइड्रोकार्बन में। कौन सा?
यह कई बांडों के माध्यम से ब्रोमीन का जोड़ है। यदि हम मानते हैं कि तीसरा सूत्र सही है, तो निम्नलिखित यौगिक प्राप्त किया जाना चाहिए: CH 2 Br-CHBr-CBr 2 -CBr 2 -CH 2 Br-CH 2 Br
यह असंतृप्त हाइड्रोकार्बन को ब्रोमीन के पानी से कई बार हिलाने के लिए पर्याप्त है, क्योंकि पीला घोल रंगहीन हो जाता है।
प्रदर्शन का अनुभव।
बेंजीन को ब्रोमीन के पानी से हिलाएं - कोई प्रभाव नहीं!
तो हमारा धारणाएं गलत हैं।
आप ब्रोमीन नहीं, बल्कि बेंजीन अणु से जुड़ने का प्रयास कर सकते हैं हाइड्रोजन।हमारी शर्तों के तहत ऐसा नहीं किया जा सकता है। लेकिन अगर यह उत्प्रेरक के ऊपर एक विशेष उपकरण में किया जाता है, तो सूत्र के साथ बेंजीन से हाइड्रोकार्बन प्राप्त करना संभव है ![]()
यदि आप इस पर ब्रोमीन जल से क्रिया करते हैं - प्रतिक्रिया नकारात्मक है।तब यह माना जाना बाकी है कि हाइड्रोकार्बन साथ में6 नहीं 12 में एक बंद चक्रीय संरचना है। इस वलय में छह CH2 समूह होते हैं:

स्पष्ट रूप से, बेंजीनभी एक चक्रीय हैसंरचना। और इसके लिए सूत्र है:

दोहरे बंधन के साथ? लेकिन ब्रोमीन पानी !???
के लिये उत्तरदयी होना मान लेनाकि एक छह-सदस्यीय वलय में एक साथ लाए गए तीन दोहरे बंधन किसी तरह व्यवहार करते हैं एक नए तरीके से।
बेंजीन सूत्र - तीन दोहरे बंधनों वाला एक षट्भुज - पुष्टि की गई संश्लेषणबेंजीन एसिटिलीन से।तीन एसिटिलीन अणु एक बेंजीन रिंग बनाते हैं। इस मामले में, एसिटिलीन के तीन बंधनों में से एक, जैसा कि यह था, दूसरे अणु के कार्बन परमाणु के साथ एक साधारण बंधन के गठन के लिए जाता है, और दो बने रहते हैं। परिणाम डबल और सिंगल बॉन्ड का एक विकल्प है।

जर्मन रसायनज्ञ फिएड्रिच ऑगस्ट केकुले ने 1865 में पहली बार इस निष्कर्ष पर पहुंचने पर इस तरह या कुछ इस तरह से तर्क दिया कि बेंजीन एक षट्भुज है जिसमें बारी-बारी से डबल और सिंगल बॉन्ड होते हैं।
तूफानी से मिले केकुले के फार्मूले बहस,जो कई दशकों से कम नहीं हुआ है। दरअसल, बेंजीन के कुछ गुण, यह सूत्र अच्छा है व्याख्या की, और कुछ विरोध किया।
यह पता चला कि बेंजीन अभी भी कुछ शर्तों के तहत, हलोजन जोड़ें,उदाहरण के लिए, सभी तीन दोहरे बंधनों में छह क्लोरीन परमाणु। दूसरी ओर, परमाणु हाइड्रोजनबेंजीन में बहुत आसानी से हो सकता है जगह ले लीअन्य समूहों के लिए (हम इस बारे में बाद में बात करेंगे)। यह क्षमता परिसर में बेंजीन के मुख्य गुणों में से एक है, जिसे कहा जाता है सुगन्धितता। सुगंध (अर्थात क्षमता हाइड्रोजन परमाणुओं को बदलना आसान)केकुले सूत्र द्वारा समझाया नहीं गया है। आगे। प्रत्येक अप्रतिस्थापित बेंजीन के लिए, इस सूत्र को देखते हुए, होना चाहिए दो समावयवी. उदाहरण के लिए, ऑर्थो-ज़ाइलीन के लिए, ये आइसोमर्स हैं:

वास्तव में कोई नहीं नहीं चुन सकाऑर्थो-ज़ाइलीन के दो समावयवी। बेंजीन की संरचना के सिद्धांत के निर्माता को अपने सूत्र में "स्पष्टीकरण" करना पड़ा। केकुले ने सुझाव दिया कि डबल कनेक्शन तय नहीं हैंबेंजीन में, लेकिन हर समय चल रहे है।

विवादबेंजीन की संरचना के सिद्धांत के आसपास रह गए हैंअभी कुछ दशक पहले। क्या हैं के बारे में आधुनिक विचारइलेक्ट्रोनिक इमारतबेंजीन?
जर्मन रसायनज्ञ ई. हकल ने सुगंधित यौगिकों के लिए क्वांटम यांत्रिक सिद्धांत लागू किया और दिखाया कि प्रत्येक कार्बन परमाणु SP² संकरित अवस्था में है। इसका क्या मतलब है?
कक्षा(ब्लैकबोर्ड पर छात्र)।

प्रत्येक कार्बन के चार इलेक्ट्रॉनों में से एक S और दो P - इलेक्ट्रॉन तीन पूरी तरह से समान SP² - हाइब्रिड ऑर्बिटल्स बनाते हैं जो एक ही विमान में एक दूसरे से 120 ° के कोण पर स्थित होते हैं। इनमें से दो ऑर्बिटल्स का उपयोग दो पड़ोसी कार्बन के समान ऑर्बिटल्स के साथ ओवरलैप करने के लिए किया जाता है, और एक का उपयोग हाइड्रोजन परमाणु के साथ करने के लिए किया जाता है।
ये सभी इलेक्ट्रॉन बनते हैं बेंजीन की इलेक्ट्रॉनिक रीढ़।

प्रत्येक कार्बन परमाणु के ऊपर और नीचे है बड़ा आंकड़ा पी - इलेक्ट्रॉन।
अब कल्पना कीजिए कि आकृति के बेंजीन वलय में आठ P - इलेक्ट्रॉन जोड़े में हैं ओवरलैप "पक्ष"वे। तीन दोहरे बंधन बनाते हैं। यह केकुले सूत्र द्वारा कागज पर वर्णित बेंजीन का इलेक्ट्रॉनिक मॉडल है। (बॉल-एंड-स्टिक मॉडल दिखाएं)।
यदि केकुले का सूत्र सही है, तो दूरीएक बेंजीन अणु में दो आसन्न कार्बन परमाणुओं के बीच भिन्न होना चाहिए: 0.154 एनएमपरमाणुओं के बीच जिसमें p-बादल ओवरलैप नहीं होते हैं और 0.133 एनएमकार्बन के बीच बाध्य पी- संचार।
लेकिन भौतिक विधियों द्वारा बेंजीन के अध्ययन से पता चला है कि अणु में सभी दूरियां सख्ती से समान हैं और सी-सी बंधन की लंबाई है 0.140 एनएम,वे। सिंगल और डबल बॉन्ड की लंबाई के बीच का औसत। यह मानना तर्कसंगत है कि प्रत्येक इलेक्ट्रॉनिक आठ एक कक्षीय है उसी को ओवरलैप करता हैऔर एक साथ दो पड़ोसियों के समान आठों के साथ।
अणु के तल पर प्रक्षेपण में, ये इलेक्ट्रॉन बादल दिखाई देंगे अतिव्यापी वृत्त(तालिका के अनुसार दिखाएं)। एक अणु में, तीन अलग नहीं पी- कनेक्शन, और एकीकृत पी- इलेक्ट्रॉनिक सिस्टमछह इलेक्ट्रॉनों में से, सभी कार्बन परमाणुओं के लिए सामान्य। अणु के लिए इस आम के प्रभाव में पी- इलेक्ट्रॉन बादल और दूरी कम हो रही हैकार्बन परमाणुओं के बीच 0.154 से 0.140 एनएम।
बेंजीन अणु का एक स्केल (वॉल्यूमेट्रिक) मॉडल तालिका (शो) में प्रस्तुत किया गया है। चूंकि इलेक्ट्रॉन घनत्व अणु में समान रूप से वितरित किया जाता है, सी परमाणुओं के बीच सभी बंधन बिल्कुल समान होते हैं।
तो रासायनिक सम्बन्धबेंजीन में, सिंगल नहीं और डबल नहीं, लेकिन जैसा कि कहने की प्रथा है डेढ़,प्रकृति में मध्यवर्ती। इन कनेक्शनों को भी कहा जाता है सुगंधित,वे मजबूत पी- सम्बन्ध(इसलिए ब्रोमीन का पानी रंगहीन नहीं होता है - ब्रोमीन परमाणु संलग्न नहीं होते हैं)।
विद्युत के समान वितरण को दर्शाने के लिए। बेंजीन अणु में घनत्व, इसका संरचनात्मक सूत्र अक्सर दर्शाया जाता है वृत्त के साथ षट्भुजअंदर:
ऐसी संरचना कहलाती है बेंजीनया सुगंधित कोर।और हाइड्रोकार्बन, अणुओं की संरचना में, जिसमें एक सुगंधित नाभिक होता है, कहा जाता है सुगंधित हाइड्रोकार्बन।
वास्तव में, बेंजीन अणु की यह संरचना पहली और दूसरी दोनों संरचनाओं की संरचनात्मक विशेषताओं को सहन करती है और गुणात्मक रूप से नई प्रणाली का प्रतिनिधित्व करती है। आइए आपके जैविक ज्ञान के आधार पर एक सादृश्य बनाएं: घोड़े और गधे का एक संकर एक खच्चर है। खच्चर में घोड़े और गधे दोनों की विशेषताएं होती हैं, लेकिन यह पूरी तरह से नया जानवर है, जिसमें केवल इसमें निहित विशेषताएं हैं। और इसलिए, यदि हम इस जानवर का वर्णन किसी ऐसे व्यक्ति से करना चाहते हैं जिसने कभी खच्चर नहीं देखा है, तो हम घोड़े के बारे में, गधे के बारे में बात कर सकते हैं, और फिर कह सकते हैं: खच्चर बीच में कुछ है।
लेकिन अब भी, केकुले सूत्र का उपयोग अक्सर किया जाता है, इस बात को ध्यान में रखते हुए कि यह केवल सशर्त रूप से अणु की संरचना को बताता है।
आइए संक्षेप करें:(ज्ञान का समेकन)
- कौन से हाइड्रोकार्बन सुगंधित कहलाते हैं?
- सुगंधित नाभिक के लिए किस प्रकार का संकरण विशिष्ट है?
- बेंजीन रिंग क्या है?
- एकता कैसे होती है पी- कनेक्शन?
- ऐरोमैटिक नाभिक में बंध दिशाओं के बीच कोण क्या होते हैं?
- कार्बन परमाणुओं के बीच की दूरी कितनी है?
- सुगंधित (डेढ़) बंध किसे कहते हैं?
सबक खत्म! अलविदा!
एरोमैटिक्स (एरेनास) - ये ऐसे कार्बनिक यौगिक हैं जिनके अणुओं में एक या एक से अधिक बेंजीन वलय होते हैं। बेंजीन रिंग, या न्यूक्लियस, कार्बन परमाणुओं का एक चक्रीय समूह है जिसमें एक विशेष प्रकृति के बंधन होते हैं।
सामान्य सूत्र- सी एन एच 2एन-6
1. प्रतिनिधि:
mononuclear
1. सी 6 एच 6 - बेंजीन, एरेनेस की समजातीय श्रृंखला का पूर्वज
2. सी 6 एच 5 - सीएच 3 - टोल्यूनि (मिथाइलबेंजीन)
3. 6 एच 5 - सीएच \u003d С एच 2 - स्टाइरीन (विनाइलबेंजीन)
4. जाइलीन (ऑर्थो-, पैरा-, मेटा-ज़ाइलीन)
मल्टीकोर (संघनित)
1. नेफ़थलीन
2.
अंगारिन
2. सुगंधित हाइड्रोकार्बन की संरचना :
बेंजीन का पहला संरचनात्मक सूत्र 1865 में जर्मन रसायनज्ञ एफ.ए. केकुले द्वारा प्रस्तावित किया गया था:

बेंजीन अणु में सी परमाणु एक नियमित सपाट षट्भुज बनाते हैं, हालांकि इसे अक्सर लम्बा खींचा जाता है।
उपरोक्त सूत्र छह सी परमाणुओं की तुल्यता को सही ढंग से दर्शाता है, लेकिन बेंजीन के कई विशेष गुणों की व्याख्या नहीं करता है। उदाहरण के लिए, असंतोष के बावजूद, यह अतिरिक्त प्रतिक्रियाओं की प्रवृत्ति नहीं दिखाता है: ब्रोमीन पानी और पोटेशियम परमैंगनेट के घोल का रंग नहीं बदलता है, अर्थात। यह असंतृप्त यौगिकों की विशिष्ट गुणात्मक प्रतिक्रियाओं की विशेषता नहीं है .
केकुले के संरचनात्मक सूत्र में, तीन सिंगल और तीन डबल अल्टरनेटिंग कार्बन-कार्बन बॉन्ड हैं। लेकिन ऐसी छवि अणु की वास्तविक संरचना को व्यक्त नहीं करती है। वास्तव में, बेंजीन में कार्बन-कार्बन बांड समतुल्य हैं। यह इसके अणु की इलेक्ट्रॉनिक संरचना के कारण है।
बेंजीन अणु में प्रत्येक C परमाणु sp 2 संकरण की अवस्था में होता है। यह दो पड़ोसी C परमाणुओं से और एक H परमाणु से तीन . से बंधा होता है σ -सम्बन्ध। नतीजतन, एक सपाट षट्भुज बनता है, जहां सभी छह सी परमाणु और सभीσ -सी-सी और सी-एच बांड एक ही तल में स्थित हैं (सी-सी बांड के बीच का कोण 120 डिग्री है)।
चावल। शिक्षा योजना बेंजीन अणु में बंधन।
कार्बन परमाणु का तीसरा p-कक्षक संकरण में शामिल नहीं है। इसमें एक डम्बल का आकार होता है और यह बेंजीन रिंग के तल के लंबवत उन्मुख होता है। पड़ोसी C परमाणुओं के ऐसे p-कक्षक वलय तल के ऊपर और नीचे अतिव्यापन करते हैं।
चावल। बेंजीन अणु में कार्बन के गैर-संकर 2p कक्षक
नतीजतन, छह पी-इलेक्ट्रॉन (सभी छह सी परमाणुओं में से) एक आम बनाते हैं π -इलेक्ट्रॉन बादल और सभी सी परमाणुओं के लिए एक ही रासायनिक बंधन।
चावल। बेंजीन अणु। जगह π - इलेक्ट्रॉन बादल
π - इलेक्ट्रॉन बादल सी परमाणुओं के बीच की दूरी में कमी का कारण बनता है।
बेंजीन अणु में, वे समान और 0.139 एनएम के बराबर होते हैं। सिंगल और डबल बॉन्ड के मामले में, ये दूरियां क्रमशः 0.154 और 0.134 एनएम होंगी। इसका मतलब यह है कि बेंजीन अणु में सरल और दोहरे बंधन का कोई विकल्प नहीं है, लेकिन एक विशेष बंधन है - "डेढ़" - एकल और दोहरे के बीच का मध्यवर्ती, तथाकथित सुगंधित बंधन। बेंजीन अणु में पी-इलेक्ट्रॉन बादल के समान वितरण को दिखाने के लिए, इसे एक नियमित षट्भुज के रूप में एक सर्कल के साथ चित्रित करना अधिक सही है (सर्कल सी परमाणुओं के बीच बांड की समानता का प्रतीक है):

3. समरूपता, नामकरण
आइसोमेरिज्म मौजूदा रेडिकल्स के कार्बन कंकाल के आइसोमेरिज्म और बेंजीन रिंग में उनकी पारस्परिक स्थिति के कारण होता है। दो प्रतिस्थापनों की स्थिति उपसर्गों द्वारा इंगित की जाती है: ऑर्थो- (ओ-) यदि वे पड़ोसी कार्बन परमाणुओं पर हैं (स्थिति 1, 2-), मेटा (एम-) एक कार्बन परमाणु (1, 3-) और . द्वारा अलग किए जाने के लिए जोड़ा- (पी-) एक दूसरे के विपरीत (1, 4-) के लिए।
उदाहरण के लिए, डाइमिथाइलबेंजीन (xylene) के लिए:
ऑर्थो-ज़ाइलीन (1,2-डाइमिथाइलबेनज़ीन)
मेटा-ज़ाइलीन (1,3-डाइमिथाइलबेनज़ीन)
पैरा-ज़ाइलीन (1,4-डाइमिथाइलबेनज़ीन)
सुगंधित हाइड्रोकार्बन मूलक कहलाते हैं एरिल रेडिकल्स . रेडिकल सी 6 एच 5 - कहा जाता है फिनाइल
