Concentrațiile maxime admise de substanțe nocive în corpurile de apă. MPC în mediul acvatic
Valabilitatea și invaliditatea utilizării diverselor liste de MPC-uri pentru Ape uzate producție de galvanizare
LA anul trecut există o oarecare creștere în Rusia productie industriala, care, pe de o parte, duce la o revigorare a producției galvanice, dar, pe de altă parte, este constrâns de pericolul ridicat pentru mediu. Instalațiile de tratare ale întreprinderilor ar trebui să servească la reducerea pericolului de mediu al producției galvanice. Cu toate acestea, pe lângă motive obiective (tehnologii de curățare învechite, starea proastă a echipamentelor etc.), există motive subiective pentru ineficacitatea măsurilor de mediu, dintre care principalele sunt utilizarea nerezonabilă a diferitelor liste de MPC-uri și reglementările regionale nerezonabile. realizarea.
Pe baza diferenței dintre scopurile consumului de apă și în cerințele diferiților consumatori de apă pentru calitatea corpurilor de apă, există atât standarde de igienă, cât și standarde de mediu pentru aceiași poluanți chimici ai apei.
MPC-urile igienice sunt concentrațiile maxime de substanțe la care nu au încă un impact direct sau indirect asupra sănătății populației (atunci când sunt expuse organismului uman pe tot parcursul vieții), iar condițiile de igienă pentru utilizarea apei nu se înrăutățesc. Standardele de igienă reglementează conținutul de poluanți numai în acele corpuri de apă care sunt utilizate în scopuri menajere și potabile și culturale și menajere, inclusiv utilizarea apei de agrement, și nu în întregul rezervor sau în locurile în care sunt evacuate ape uzate, ci numai în punctele de utilizare a apei din populaţia cea mai apropiată de scurgerile de evacuare. Există două categorii de gospodărie și de băut și utilizarea culturală și comunitară a apei: prima categorie include utilizarea unui corp de apă ca sursă de alimentare cu apă menajeră și potabilă, precum și pentru alimentarea cu apă a întreprinderilor din industria potabilă; la a doua categorie - utilizarea corp de apaîn scopuri culturale și cotidiene ale populației, recreere și sport.
Apariția de noi surse de poluare și extinderea geografiei lor au dus la dezvoltarea sistem independent MPC pentru pescuit (de mediu) care vizează protejarea corpurilor de apă ca bază pentru piscicultură și pescuit organizate. Există două categorii de utilizare a apei pentru pescuit: prima categorie include utilizarea unui corp de apă pentru conservarea și reproducerea speciilor de pești valoroși care sunt foarte sensibili la oxigen; la al doilea - utilizarea unui corp de apă pentru producția comercială de pești și alte animale și plante acvatice.
Dacă rezervorul este folosit în scopuri de pescuit și pentru alimentarea cu apă a populației, acestea sunt ghidate de cel mai strict standard.
La atribuirea unui corp de apă la o anumită categorie, organele Comitetului de Stat pentru Pescuit sunt ghidate de Decretul Consiliului de Miniștri al URSS nr. 1045 din 15 septembrie 1958, conform căruia: „Toate rezervoarele și apele lor accesorii care sunt utilizate sau pot fi utilizate pentru producția comercială de pește și alte animale și plante acvatice sau sunt importante pentru reproducerea stocurilor de pești comerciale, sunt considerate rezervoare de pescuit. Astfel, în conformitate cu o astfel de definiție nejustificat de largă, toate corpurile de apă de suprafață ale unei țări atât de uriașe precum Rusia sunt clasificate drept corpuri de apă pentru pescuit, adică se presupune că în toate suprafata apei Oemurile Rusiei sunt păstrate și reproduse specii valoroase pești cu o sensibilitate ridicată la oxigen sau sunt utilizați pentru producția comercială de pește și alte animale și plante acvatice. Rezultă că, în toate cazurile, apele de suprafață trebuie controlate conform MAC pentru corpurile de apă piscicole (MAC RH).
În plus, deoarece aproape toate punctele de evacuare a apelor uzate sunt situate în limitele unei așezări, în conformitate cu regulile și normele de protecție a apelor de suprafață, standardele pentru poluarea maximă a corpurilor de apă se aplică apelor deversate în sine, adică, diluarea efluenților în apa unui rezervor și capacitatea de asimilare a rezervoarelor nu sunt luate în considerare. Astfel, cerințele listei MPC de RH sunt aplicate universal la calitatea apelor uzate evacuate în corpurile de apă.
Mai mult, astfel de cerințe sunt impuse nu numai efluenților urbani deversați în corpurile de apă, ci și efluenților care intră în canalizarea orașului de la întreprinderi. Astfel, nu numai diluarea apelor uzate industriale este urbană gunoi menajer, dar transferă și ineficiența funcționării stațiilor urbane de epurare pe umerii întreprinderilor. Acest lucru înăsprește în mod nerezonabil și inutil cerințele pentru calitatea apelor uzate de la întreprinderi și le duce într-o fundătură din cauza realizării, evident imposibile, a unor astfel de MPC-uri folosind tehnologii standard de tratare a apelor uzate pentru producția galvanică.
Să susținem această afirmație.
Practic la toate statiile de tratare a apelor uzate de productie galvanica se foloseste metoda reactivului. Principalii poluanți ai acestor ape uzate sunt ionii de metale grele. Concentrația reziduală a ionilor de metale grele, atât calculată din produsul solubilității hidroxizilor corespunzători, cât și observată în practică, este prezentată în Tabelul 1.
Tabelul 1. Eficiența metodei reactiv pentru tratarea apelor uzate din metale grele
| ion de metal greu | Concentrația de ioni metalici reziduali calculată din produsul de solubilitate, mg/l | Concentrația de ioni metalici reziduali observată în practică la pH 8,5-9,0, mg/l | MPC RH, mg/l |
| Fe2+ | 0,44 | 0,3 - 1 | 0,1 |
| Fe3+ | 0,21 10 -4 | 0,3 - 0,5 | 0,1 |
| * Cr3+ | 0,13 10 -2 | 0,05 - 0,1 | 0,07 |
| Cu2+ | 0,024 | 0,1 - 0,15 | 0,001 |
| Ni2+ | 1,47 | 0,25 - 0,75 | 0,01 |
| Zn2+ | 0,17 | 0,05 - 0,1 | 0,01 |
| CD 2+ | 2,62 | 2,5 | 0,005 |
| Al 3+ | 0,23 10 -3 | 0,1 - 0,5 | 0,04 |
* - nu se dau date despre Cr 6+, deoarece în stadiul de neutralizare a efluenților care conțin crom, reacția de reducere chimică a Cr 6+ la Cr 3+ are loc complet.
Orez. 1. Schema de aplicare a diverselor liste de MPC în apele uzate
Prin urmare, există trei puncte de-a lungul întregii lungimi a sistemului de canalizare menajeră în orice oraș în care diferite liste MPC trebuie aplicate apelor uzate (Fig. 1), așa cum se face la Moscova (descris mai jos):
1 - la iesirea din intreprindere - concentrarea maxima Substanțe dăunătoareîn apele uzate admise în sistemul de canalizare al orașului;
2 - inainte de a intra in statiile orasului tratament biologic- concentrația admisibilă de substanțe nocive în apele uzate acceptate pentru epurare biologică;
3 - la locul deversării apelor uzate într-un rezervor natural în conformitate cu categoria sa - fie MPC-ul substanțelor nocive din apa corpurilor de apă în scopuri potabile și culturale, fie MPC-ul în apa corpurilor de apă în scopuri piscicole (MAC RH).
Să luăm în considerare utilizarea diferitelor liste de MPC pentru metale grele în apele uzate, folosind exemplul Moscovei (Fig. 2).
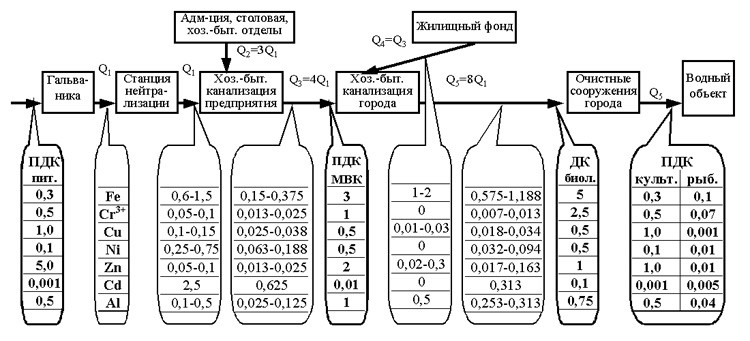
Orez. Fig. 2. Schema modificărilor concentrației ionilor de metale grele din apele uzate de la atelierul de galvanizare până la corpul de apă
(Q este volumul de apă uzată)
La întreprindere, apele uzate din producția galvanică (Q 1), care conțin ioni de metale grele, sunt supuse unui tratament chimic la stația de neutralizare, în urma căruia concentrația de ioni de metale grele atinge valorile indicate în tabelul.1. După epurare, apele uzate din producția galvanică (Q 1) sunt diluate cu ape uzate menajere (Q 2) de la administrație, gospodărie și alte departamente ale întreprinderii care nu poluează apele uzate cu ioni de metale grele. De regulă, volumul consumului de apă (eliminarea apei) al producției de galvanizare este de aproximativ 25% din consumul total de apă (eliminarea apei) al întreprinderii (Q 3). În consecință, concentrația ionilor de metale grele la ieșirea întreprinderii este de 4 ori mai mică decât concentrația acestora în apele uzate galvanice care au trecut prin instalațiile de epurare. Odată cu eficiența normală (de proiectare) a instalațiilor de tratare, concentrația reală de metale grele în sistemul de canalizare menajeră la ieșirea din întreprindere (Q 3) va fi: Fe 2+ 0,075-0,250 mg/l, Fe 3+ 0,075 -0,125 mg/l, (Fetotal 0,150-0,375 mg/l), Cr 3+ 0,013-0,025 mg/l, Cu 2+ 0,025-0,038 mg/l, Ni 2+ 0,063-0,188 mg/l, Zn 2+ 0,013+ . -0,025 mg/l, Cd2+ 0,625 mg/l, Al3+ 0,025-0,125 mg/l.
Conform „Regulilor pentru acceptarea apelor uzate industriale în canalizarea orașului Moscova (temporar)” nr. 127, aprobate prin decizia Comitetului Executiv al Consiliului de la Moscova din 20 ianuarie 1984, Mosvodokanal stabilește următoarele concentrații maxime de grele metale din apele uzate acceptate în sistemul de canalizare al orașului (în Fig. 2 MPC MVK): Fetot. 3,0 mg/l; Cr3+ 1,0 mg/l; Cu 2+ 0,5 mg/l; Ni 2+ 0,5 mg/l; Zn2+ 2,0 mg/l; Cd2+ 0,01 mg/l; Al3+ 1,0 mg/l.
Astfel, la Moscova, apele uzate provenite de la întreprinderi în sistemul municipal de canalizare, cu eficiență normală (proiectată) de funcționare a stațiilor de epurare a apelor uzate pentru tratarea apelor uzate din producția galvanică, îndeplinesc cerințele MPC (cu excepția cadmiului) stabilite de Mosvodokanal. . Reducerea concentrației de cadmiu în apele uzate ale întreprinderilor din Moscova se realizează prin limitarea utilizării cadmiului în conformitate cu Decretul Guvernului Moscovei nr. 893 din 05.11.96.
În canalizarea menajeră a orașului, apele uzate de la întreprinderi (Q 3) sunt amestecate cu apele uzate menajere din fondul locativ al orașului (Q 4), în care posibilele concentrații de metale grele sunt următoarele: Fetot. 1-2 mg/l; Cr3+ 0 mg/l; Cu2+ 0,01-0,03 mg/l; Ni 2+ 0 mg/l; Zn2+ 0,02-0,3 mg/l; Cd2+ 0 mg/l; Al3+ 0,5 mg/l. Cu condiția ca volumul zilnic de ape uzate industriale să poată atinge maximum 50% din debitul total de ape uzate al orașului, concentrația de metale grele în efluenți amestecați. ![]() nu este mai mult de: Fegen. - 0,575-1,188 mg/l; Cr3+ - 0,007-0,013 mg/l; Cu 2+ - 0,018-0,034 mg/l; Ni 2+ - 0,032-0,094 mg/l; Zn2+ - 0,017-0,163 mg/l; Cd2+ - 0,313 mg/l; Al3+ - 0,253-0,313 mg/l.
nu este mai mult de: Fegen. - 0,575-1,188 mg/l; Cr3+ - 0,007-0,013 mg/l; Cu 2+ - 0,018-0,034 mg/l; Ni 2+ - 0,032-0,094 mg/l; Zn2+ - 0,017-0,163 mg/l; Cd2+ - 0,313 mg/l; Al3+ - 0,253-0,313 mg/l.
Efluenții amestecați (Q5) cu această concentrație de metale grele sunt trimiși la stațiile de epurare biologică municipale. Conform regulilor de admitere apa industrialaîn sistemele de canalizare aşezări„Concentrația admisibilă de metale grele în apele uzate acceptată pentru epurare biologică este: Fetotal 5,0 mg/l; Cr 3+ 2,5 mg/l; Cu 2+ 0,5 mg/l; Ni 2+ 0, 5 mg/l, Zn 2+ 1,0 mg/l, Cd 2+ 0,1 mg/l, Al 3+ 0,75 mg/l și apele uzate menajere, îndeplinesc lista concentrațiilor admise de metale grele (cu excepția cadmiului) pentru tratarea biologică.
Practica a demonstrat că în procesul de epurare biologică a apelor uzate are loc o scădere semnificativă a concentrației ionilor de metale grele (cu 40-80%) datorită absorbției acestora de către nămolul activ. Dar chiar și fără a ține cont de acest lucru, efluenții urbani (Q 5) care conțin ape uzate industriale și menajere, în ceea ce privește concentrația de ioni de metale grele, îndeplinesc cerințele listei MPC-urilor de substanțe nocive (cu excepția fierului și a cadmiului) în băut. apă și scopuri culturale și casnice. Excesul de conținut de fier în efluenți față de CPM în scopuri culturale și casnice este determinat de contribuția covârșitoare la acest exces de contaminare cu fier a efluenților domestici.
Aplicarea cerințelor listei MPC în scop cultural și comunitar la apele uzate urbane este corectă din punct de vedere logic, pe baza tezei: „scurgerile ar trebui controlate conform aceleiași liste de MPC, conform căreia apa furnizată întreprinderilor și rezidențiale. sectorul este controlat”. Mai mult decât atât, MPC-ul ITM în apă potabilă (MPCp.) coincide practic cu MPC-ul lor în apă pentru uz casnic și potabil și cultural
Ținând cont de faptul că nici râul Moscova, nici Yauza, nici alte râuri ale Moscovei, cu toată dorința, nu pot fi atribuite corpurilor de apă pentru pescuit, cerințele regulilor și reglementărilor pentru protecția apelor de suprafață împotriva poluării de către apele uzate din producția galvanică din Moscova sunt destul de realizabile. Pentru aceasta, este necesar să se asigure munca normala statii de neutralizare. Dacă volumul efluenților galvanici depășește 25% din consumul total de apă al întreprinderii, atunci pentru a îndeplini aceste cerințe, este necesar să se reducă consumul de apă pentru spălare în magazinele de galvanizare și/sau să se introducă instalații locale pentru curățarea apa de spalat.
Cu toate acestea, cerințele listei MPC pentru rezervoarele de pescuit sunt aplicate universal efluenților deversați în corpurile de apă și chiar efluenților întreprinderilor care intră în canalizarea orașului, ceea ce face de fapt imposibilă evacuarea apei potabile în apele uzate fără epurare. Absurditatea cerințelor de tratare a apelor uzate de la întreprinderi la o puritate mai profundă decât puritatea bând apă, cu greu poate fi pusă la îndoială. Cu toate acestea, astăzi toate cerințele pentru întreprinderi privind puritatea efluenților sunt de fapt reduse (deși într-o formă oarecum acoperită) la faptul că efluenții sunt mult mai curați decât apa furnizată întreprinderii. Un alt contraargument major la aplicarea MPC pentru rezervoarele de pescuit la apele uzate industriale este imposibilitatea practică de a obține o asemenea puritate a apelor uzate prin oricare dintre metodele cunoscute. „Practic” în sensul că utilizarea multor metode de post-epurare a apelor uzate face ca funcționarea întreprinderilor industriale să fie nejustificată din punct de vedere economic. Astfel, însuși faptul prezenței producției galvanice ca parte a întreprinderii o face o încălcare a legislației de mediu.
Această situație este exacerbată de stabilirea voluntaristă a regulilor regionale. În multe regiuni, cerințele pentru apele uzate de la întreprinderi sunt mult mai stricte decât chiar și MPC pentru corpurile de apă pentru pescuit. De exemplu, în conformitate cu prevederea „Instrucțiuni pentru reglementarea emisiilor (evacuărilor) de poluanți în atmosferă și în corpurile de apă”, aprobată de vicepreședintele URSS Goskompriroda la 11 septembrie 1989, în cazul în care evacuarea efectivă de substanțe cu apa uzată este mai mică decât debitul maxim admisibil calculat (MPD) , atunci deversarea reală este luată ca PDS (clauza 3.4). Această prevedere este interpretată de autoritățile regionale de mediu într-o manieră simplă, fără a ține cont de scopul principal al stabilirii standardelor MPD - inadmisibilitatea depășirii MPC stabilite. documente normative nivel federal, sau dacă acestea sunt depășite sub influența factorilor naturali de conservare (nu de deteriorare) a compoziției și proprietăților apei unui rezervor natural. Prin urmare, autoritățile regionale își permit să stabilească standarde de calitate pentru efluenții întreprinderilor la un nivel practic apă curată, de exemplu, dacă în timpul prelevării probelor la întreprindere, dintr-un anumit motiv (timp de oprire a producției, repararea echipamentelor etc.), nu s-au format efluenți poluați. Asemenea acțiuni ale autorităților regionale de mediu pentru a stabili MPD, inclusiv cele bazate pe principiul „de la nivelul atins” (de exemplu, ca urmare a creșterii eficienței instalațiilor de tratare), afectează negativ interesul întreprinderilor pentru îmbunătățirea calității apelor uzate. tratament.
Inițiativa regională de stabilire a standardelor de calitate a apelor uzate ajunge adesea la punctul de absurditate. Deci, de exemplu, în orașul Kaluga, MPC-ul zincului din apele uzate trimise la canalizarea menajeră este de 3 ori mai mic decât MPC-ul zincului din apele uzate. canalizare de furtună. Și asta având în vedere faptul că scurgerile pluviale sunt deversate direct în râul Oka, iar înainte de a fi evacuate într-un rezervor natural, apele uzate menajere sunt diluate cu apele uzate menajere din clădirile rezidențiale urbane și sunt tratate la nivel urban. facilitati de tratament.
Ca exemplu, Tabelul 2 prezintă date comparative privind MPC-urile ionilor de metale grele din efluenții evacuați de întreprinderi în canalizările orașelor, utilizați în diferite țări și orașe.
Tabelul prezentat arată că nu numai considerentele noastre descrise mai sus, ci și practica altor țări arată rigiditatea extremă nerezonabilă a cerințelor privind calitatea apelor uzate de la întreprinderile rusești. Și asta în ciuda faptului că, în ciuda cerințelor de mii de ori mai puțin stricte din Europa și Statele Unite (Tabel. 2), în ultimele decenii s-a înregistrat o revigorare a râului Rin și o scădere bruscă a poluării Marilor Lacuri Americane, unde pescuitul comercial este deja permis, iar la noi, chiar și ținând cont de scăderea producției industriale, nu s-au înregistrat progrese semnificative în îmbunătățirea starea resurselor de apă.
Tabelul 2. MPC ale metalelor grele din apele uzate evacuate de întreprinderi în canalizările orașului, utilizate în diferite țări și orașe
| Oraș de țară | Cu2+ | Zn2+ | Ni2+ | Cr3+ | Fe (total) |
| STATELE UNITE ALE AMERICII | 2,07 | 1,48 | 2,38 | - | - |
| Germania | 0,5 | 2 | 0,5 | - | 3 |
| Austria | 0,5 | 2 | 0,5 | 0,5 | - |
| Uniunea Europeană, UE | 0,5 | 0,5 | 0,5 | 0,5 | - |
| Lituania | 1 | 1 | 0,5 | 1 | - |
| Belarus, Minsk | 1 | 5 | 0,44 | 2,5 | 3,3 |
| Federația Rusă | |||||
| Kirzhach | 0,0001 | 0,001 | 0,001 | 0,014 | 0,006 |
| Kaluga | 0,0026 | 0,0036 | 0,012 | 0,029 | 1,98 |
| Mtsensk | 0,0009 | 0,04 | 0,028 | 0,01 | 0,1 |
| Tula | 0,0125 | 0,06 | 0,04 | 0,1 | 3,0 |
| Kazan | 0,08 | 0,066 | 0,01 | 0,4 | 0,6 |
| Vultur | 0,01 | 0,08 | 0,06 | 3,6 | 1 |
| Izhevsk | 0,23 | 0,21 | 0,04 | 1,35 | 0,4 |
| Serghiev Posad | 0,73 | 0,11 | 0,14 | 2,4 | 1,2 |
| Moscova | 0,5 | 2 | 0,5 | 1 | 3 |
| MPC pentru apă potabilă | 1 | 5 | 0,1 | 0,5 | 0,3 |
| MPC pentru rezervoare de apă menajeră și potabilă și culturală și menajeră | 1 | 1 | 0,1 | 0,5 | 0,3 |
| MPC pentru rezervoare de pescuit | 0,001 | 0,01 | 0,01 | 0,07 | 0,1 |
În consecință, scopul nu este în reducerea efectivă a MPC în efluenții industriali, ci într-o abordare diferită a menținerii calității. mediu inconjurator. În majoritatea țărilor industrializate, o întreprindere utilizator de apă a stabilit astfel de standarde de calitate a apelor uzate pe care le poate îndeplini la instalațiile de tratare a apelor uzate existente, iar aceste standarde sunt aceleași pentru toate instalațiile de anumite tipuri și capacități. Prin urmare, standardele stabilite sunt destul de realizabile și vizează ca toți (fără excepție) utilizatorii de apă să nu depășească normele stabilite și să poarte responsabilitatea pentru încălcările lor. În plus, atunci când sunt vândute la stațiile de tratare a apelor uzate, mai mult decât tehnologii eficienteîntreprinderile de curățenie fac obiectul unor măsuri de stimulare și scutiri fiscale, ceea ce face ca afacerea să devină un actor de mediu.
Imposibilitatea fundamentală de executare cerințele de reglementare la calitatea apelor uzate în regiunile Federației Ruse, chiar și atunci când se implementează cel mai mult tehnologii moderne curățenia transformă aproape 100% din întreprinderi în încălcări ale legii naturale și le privează complet de stimulentul de a îmbunătăți situația de mediu. Cerințele nerezonabil de dure și nerealiste, taxele inechitabile de poluare, amenzile și sancțiunile pun întreprinderile în pragul falimentului.
Toate acestea sugerează că este necesară schimbarea semnificativă a sistemului de gestionare a calității apei și a resurselor de apă la nivel federal și regional, precum și a legislației privind apa. Această problemă a fost ridicată în mod repetat în presă, inclusiv pe paginile revistelor „Aprovizionare cu apă și inginerie sanitară” și
Elementele dăunătoare sunt standardul normelor sanitare și igienice stabilite prin acte de stat. Nerespectarea valorilor limită specificate în acesta constituie infracțiune pentru care infractorii sunt trași la răspundere în condițiile legii. Standardul MPC în apă oferă instrucțiuni cu privire la acele valori limită ale poluanților, al căror conținut nu implică daune pentru sănătatea sau viața umană.
Principalele surse de elemente toxice sunt numeroasele întreprinderi funcționale ale complexului industrial. Emisiile lor sunt suficient de puternice pentru sol și apă. Elemente chimice care au influenta negativa asupra mediului din jurul nostru, se obișnuiește să se împartă în grupuri în funcție de gradul de pericol pentru oameni. Acestea includ substanțe periculoase:
de urgență;
înalt;
Moderat.
Există, de asemenea, un grup de elemente periculoase.
MPC-urile din diverse ape sunt reflectate în tabele special concepute. Există, de asemenea, diverse formule, a căror utilizare vă permite să calculați toleranță limită toxine. Acestea sunt folosite de specialiști pentru a efectua măsuri de control pentru apa folosită de om. Astfel de acțiuni pot fi efectuate de oricare dintre noi. Pentru a face acest lucru, este suficient să analizați starea apei potabile din casa dvs. și să o comparați cu standarde acceptabile fiind în ea diverse elemente. De exemplu, conținutul în miligrame pe litru nu trebuie să fie mai mare decât:
Reziduu uscat - 1000;
Sulfați - 500;
Cloruri - 350;
Zinc - 5;
Fier - 0,3;
Mangan - 0,1;
Polifosfați reziduali - 3.5.
Totalul nu trebuie să depășească șapte miligrame pe litru.
Mare importanță are de asemenea control asupra stării solului. Este pământul care servește ca acumulator și filtru pentru diferite conexiuni. MPC-urile care sunt descărcate în mod constant în sol trebuie, de asemenea, să respecte standardele, deoarece migrarea constantă în acesta straturile superioare poluează grav întregul mediu.
În funcție de sol, nu poate fi mai mult de:
0,02 mg/kg benzapiren;
3 mg/kg cupru;
130 mg/kg nitrați;
0,3 mg/kg toluen;
23 mg/kg zinc.
În cazul depășirii CPM în apă, autoritățile implicate în monitorizarea stării mediului vor stabili cauza acestui fenomen. Destul de des, la o creștere a cantității în natură substanțe chimice afectate de deșeurile menajere obișnuite. În prezent, problema curățării corpurilor de apă de compuși de fosfat și azot este deosebit de acută. Trei abordări diferite pot fi utilizate pentru a rezolva această problemă:
Chimic;
Biologic;
O combinație a primelor două metode.
Aducerea la valoarea standard a MPC în apă folosind curatare chimica presupune formarea de fosfați metalici, care, fiind insolubili, se depun la fund recipient special. Acest proces are loc cu ajutorul reactivilor. Folosind metoda de curățare chimică găsește aplicare largă pe întreprinderile industriale. Această lucrare poate fi efectuată numai de personal special instruit.
Dacă în purificarea apei se utilizează fosfor sau bacterii P, atunci această metodă este biologică. Aceasta este o abordare naturală modernă pentru prevenirea excesului de MPC. Zonele speciale ale rezervoarelor de tratare sunt alimentate alternativ cu aerobic și bacterii anaerobe. Această metodă este utilizată în biofiltre, fose septice și rezervoare de aerare.
Combinația dintre biologice și metode chimice utilizat în sistemele de tratare, unde este nevoie de accelerarea și intensificarea reacțiilor de descompunere a apelor uzate.
Substanțe toxice foarte periculoase. În zilele noastre, monitorizarea nivelurilor diferitelor astfel de substanțe este deosebit de importantă în zonele industriale și urbane.
Deși toată lumea știe ce sunt metalele grele, nu toată lumea știe ce elemente chimice inca se încadrează în această categorie. Există multe criterii după care diferiți oameni de știință definesc metalele grele: toxicitatea, densitatea, masa atomică, ciclurile biochimice și geochimice, distribuția în natură. Conform unui criteriu, metalele grele includ arsenul (un metaloid) și bismutul (un metal fragil).
Date generale despre metalele grele
Sunt cunoscute peste 40 de elemente care sunt clasificate drept metale grele. Au o masă atomică mai mare de 50 a.u. Oricât de ciudat ar părea, aceste elemente sunt extrem de toxice chiar și la un cumul scăzut pentru organismele vii. V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Mo...Pb, Hg, U, Th... toate se încadrează în această categorie. Chiar și cu toxicitatea lor, multe dintre ele sunt importante în afară de cadmiul, mercurul, plumbul și bismutul pentru care nu a fost găsit niciun rol biologic.
Conform unei alte clasificari (si anume N. Reimers), metalele grele sunt elemente care au o densitate mai mare de 8 g/cm3. Astfel, vor fi mai puține dintre aceste elemente: Pb, Zn, Bi, Sn, Cd, Cu, Ni, Co, Sb.
Teoretic, metalele grele pot fi numite întregul tabel periodic al elementelor începând cu vanadiu, dar cercetătorii ne demonstrează că acest lucru nu este în întregime adevărat. O astfel de teorie se datorează faptului că nu toate sunt prezente în natură în limite toxice, iar confuzia în procesele biologice este minimă pentru mulți. Acesta este motivul pentru care mulți includ doar plumbul, mercurul, cadmiul și arsenul în această categorie. Comisia Economică pentru Europa a Națiunilor Unite nu este de acord cu această opinie și consideră că metalele grele sunt zincul, arsenul, seleniul și antimoniul. Același N. Reimers crede că prin eliminarea elementelor rare și nobile din tabelul periodic, metalele grele rămân. Dar nici aceasta nu este o regulă, alții adaugă în această clasă aur, platină, argint, wolfram, fier, mangan. De aceea va spun ca inca nu este clar acest subiect...
Discutarea echilibrului ionilor diverse substanțeîn soluție, vom descoperi că solubilitatea unor astfel de particule este legată de mulți factori. Principalii factori de solubilizare sunt pH-ul, prezența liganzilor în soluție și potențialul redox. Sunt implicați în procesele de oxidare a acestor elemente de la o stare de oxidare la alta, în care solubilitatea ionului în soluție este mai mare.
În funcție de natura ionilor, în soluție pot apărea diferite procese:
- hidroliză,
- formare complexă cu diferiți liganzi;
- polimerizare hidrolitică.
Datorită acestor procese, ionii pot precipita sau pot rămâne stabili în soluție. Proprietățile catalitice ale unui anumit element și disponibilitatea lui pentru organismele vii depind de aceasta.
Multe metale grele formează complexe destul de stabile cu substanțele organice. Aceste complexe fac parte din mecanismul de migrare a acestor elemente în iazuri. Aproape toți chelații de metale grele sunt stabili în soluție. De asemenea, complexe de acizi din sol cu săruri diferite metale(molibden, cupru, uraniu, aluminiu, fier, titan, vanadiu) au o solubilitate bună în medii neutre, ușor alcaline și ușor acide. Acest fapt este foarte important, deoarece astfel de complexe se pot deplasa în stare dizolvată la distante lungi. Cele mai vulnerabile resurse de apă sunt corpurile de apă slab mineralizate și de suprafață, unde nu are loc formarea altor astfel de complexe. Pentru a înțelege factorii care reglează nivelul unui element chimic în râuri și lacuri, reactivitatea chimică, biodisponibilitatea și toxicitatea acestora, este necesar să se cunoască nu numai conținutul total, ci și proporția formelor libere și legate ale metalului.
Ca urmare a migrării metalelor grele în complexe metalice în soluție, pot apărea următoarele consecințe:
- În primul rând, cumularea ionilor unui element chimic crește datorită trecerii acestora de la sedimentele de fund la soluțiile naturale;
- În al doilea rând, există posibilitatea de a modifica permeabilitatea membranei complexelor rezultate, spre deosebire de ionii convenționali;
- De asemenea, toxicitatea unui element în formă complexă poate diferi de forma ionică obișnuită.
De exemplu, cadmiul, mercurul și cuprul în forme chelate au o toxicitate mai mică decât ionii liberi. De aceea este greșit să vorbim despre toxicitate, biodisponibilitate, reactivitate chimică numai prin conținutul total al unui anumit element, fără a ține cont de proporția formelor libere și legate ale unui element chimic.
De unde provin metalele grele din mediul nostru? Motivele prezenței unor astfel de elemente pot fi apele uzate din diferite instalații industriale angajat în metalurgia feroasă și neferoasă, inginerie mecanică, galvanizare. Unele substanțe chimice se găsesc în pesticide și îngrășăminte și astfel pot fi o sursă de poluare pentru iazurile locale.
Și dacă intri în secretele chimiei, atunci principalul vinovat în creșterea nivelului de săruri solubile ale metalelor grele este ploaia acidă (acidificarea). O scădere a acidității mediului (o scădere a pH-ului) implică trecerea metalelor grele de la compușii slab solubili (hidroxizi, carbonați, sulfați) la cei mai ușor solubili (nitrați, hidrosulfați, nitriți, bicarbonați, cloruri) în sol. soluţie.
Vanadiu (V)
Trebuie remarcat în primul rând că contaminarea cu acest element prin mijloace naturale este puțin probabilă, deoarece acest element este foarte dispersat în Scoarta terestra. Se găsește în natură în asfalturi, bitumuri, cărbuni, minereuri de fier. Petrolul este o sursă importantă de poluare.
Conținutul de vanadiu din rezervoarele naturale
Rezervoarele naturale conțin o cantitate nesemnificativă de vanadiu:
- în râuri - 0,2 - 4,5 mcg / l,
- în mări (în medie) - 2 µg/l.
Complecșii anionici (V 10 O 26) 6- și (V 4 O 12) 4- sunt foarte importanți în procesele de tranziție a vanadiului în stare dizolvată. Complexele de vanadiu solubile cu substanțe organice, cum ar fi acizii humici, sunt, de asemenea, foarte importante.
Concentrația maximă admisă de vanadiu pentru mediul acvatic
Vanadiul în doze mari este foarte dăunător pentru oameni. Concentrația maximă admisă pentru mediul acvatic (MAC) este de 0,1 mg/l, iar în iazurile piscicole, MAC-ul fermei piscicole este și mai mic - 0,001 mg/l.
Bismut (Bi)
În principal, bismutul poate pătrunde în râuri și lacuri ca urmare a proceselor de leșiere a mineralelor care conțin bismut. Există și surse artificiale de poluare cu acest element. Acestea pot fi fabrici de sticlă, parfumuri și produse farmaceutice.
Conținutul de bismut din rezervoarele naturale
- Râurile și lacurile conțin mai puțin de un microgram de bismut pe litru.
- Dar Apele subterane poate conține chiar și 20 µg/l.
- În mări, bismutul, de regulă, nu depășește 0,02 µg/l.
Concentrația maximă admisă de bismut pentru mediul acvatic
Concentrația maximă admisă de bismut pentru mediul acvatic este de 0,1 mg/l.
Fier (Fe)
Fier - element chimic nu este rar, este conținut în multe minerale și roci și, astfel, în rezervoarele naturale nivelul acestui element este mai mare decât al altor metale. Poate apărea ca urmare a proceselor de intemperii. stânci, distrugerea acestor roci și dizolvarea. Formând diverse complexe cu substanțe organice dintr-o soluție, fierul poate fi în stări coloidale, dizolvate și suspendate. Este imposibil să nu menționăm sursele antropice de poluare cu fier. Apele reziduale din fabricile metalurgice, de prelucrare a metalelor, de vopsele și lacuri și textile, uneori, depășesc din cauza excesului de fier.
Cantitatea de fier din râuri și lacuri depinde de compoziție chimică soluție, pH și parțial pe temperatură. Formele ponderate ale compușilor de fier au o dimensiune mai mare de 0,45 μg. Principalele substanțe care fac parte din aceste particule sunt suspensiile cu compuși de fier absorbit, oxid de fier hidrat și alte minerale care conțin fier. Particulele mai mici, adică formele coloidale de fier, sunt considerate împreună cu compușii de fier dizolvați. Fierul în stare dizolvată este format din ioni, hidroxocomplexuri și complexe. În funcție de valență, se observă că Fe(II) migrează sub formă ionică, în timp ce Fe(III) rămâne în stare dizolvată în absența diferitelor complexe.
În echilibrul compușilor de fier într-o soluție apoasă, este foarte important și rolul proceselor de oxidare, atât chimice, cât și biochimice (bacteriile fierului). Aceste bacterii sunt responsabile pentru trecerea ionilor de fier Fe(II) la starea Fe(III). Compușii ferici tind să hidrolizeze și să precipite Fe(OH)3. Atât Fe(II) cât și Fe(III) tind să formeze hidroxocomplexuri ca - , + , 3+ , 4+ , + , în funcție de aciditatea soluției. LA conditii normaleîn râuri și lacuri, Fe(III) sunt asociate cu diverse substanțe anorganice și organice dizolvate. La pH mai mare de 8, Fe(III) se transformă în Fe(OH)3. Formele coloidale ale compușilor de fier sunt cele mai puțin studiate.
Conținutul de fier în apele naturale
În râuri și lacuri, nivelul de fier fluctuează la nivelul de n * 0,1 mg/l, dar poate crește în apropierea mlaștinilor la câțiva mg/l. În mlaștini, fierul este concentrat sub formă de săruri humate (săruri ale acizilor humici).
Rezervoarele subterane cu pH scăzut conțin cantități record de fier - până la câteva sute de miligrame pe litru.
Fierul este un oligoelement important și de el depind diverse procese biologice importante. Afectează intensitatea dezvoltării fitoplanctonului și de aceasta depinde calitatea microflorei din corpurile de apă.
Nivelul fierului din râuri și lacuri este sezonier. Cele mai mari concentrații în corpurile de apă se observă iarna și vara din cauza stagnării apei, dar primăvara și toamna nivelul acestui element scade vizibil din cauza amestecării maselor de apă.
Astfel, o cantitate mare de oxigen duce la oxidarea fierului din forma divalentă în forma trivalentă, formând hidroxid de fier, care precipită.
Concentrația maximă admisă de fier pentru mediul acvatic
Apa cu o cantitate mare de fier (mai mult de 1-2 mg/l) se caracterizează prin săracă palatabilitatea. Are un gust astringent neplăcut și nu este potrivit pentru scopuri industriale.
MPC-ul fierului pentru mediul acvatic este de 0,3 mg/l, iar în iazurile piscicole, MPC-ul fermelor piscicole este de 0,1 mg/l.
Cadmiu (Cd)
Contaminarea cu cadmiu poate apărea în timpul levigarii solului, în timpul descompunerii diferitelor microorganisme care îl acumulează și, de asemenea, datorită migrării din minereurile de cupru și polimetalice.
Omul este, de asemenea, vinovat pentru contaminarea cu acest metal. Apele uzate de la diverse întreprinderi care desfășoară activități de prelucrare a minereurilor, producție galvanică, chimică, metalurgică pot conține cantități mari de compuși de cadmiu.
Procesele naturale de reducere a nivelului de compuși ai cadmiului sunt sorbția, consumul acestuia de către microorganisme și precipitarea carbonatului de cadmiu slab solubil.
În soluție, cadmiul este, de regulă, sub formă de complexe organo-minerale și minerale. Substanțele sorbite pe bază de cadmiu sunt cele mai importante forme în suspensie ale acestui element. Migrația cadmiului în organismele vii (hidrobioniți) este foarte importantă.
Conținutul de cadmiu în corpurile naturale de apă
Nivelul de cadmiu din râurile și lacurile curate fluctuează la un nivel mai mic de un microgram pe litru, în apele poluate nivelul acestui element atinge câteva micrograme pe litru.
Unii cercetători cred că cadmiul, în cantități mici, poate fi important pentru dezvoltarea normală a animalelor și a oamenilor. Concentrațiile crescute de cadmiu sunt foarte periculoase pentru organismele vii.
Concentrația maximă admisă de cadmiu pentru mediul acvatic
MPC pentru mediul acvatic nu depășește 1 µg/l, iar în iazurile de pescuit, MPC pentru fermele piscicole este mai mic de 0,5 µg/l.
Cobalt (Co)
Râurile și lacurile pot fi contaminate cu cobalt ca urmare a leșierii cuprului și a altor minereuri, din sol în timpul descompunerii organismelor dispărute (animale și plante) și, bineînțeles, ca urmare a activității întreprinderilor chimice, metalurgice și de prelucrare a metalelor. .
Principalele forme de compuși de cobalt sunt în stare dizolvată și suspendată. Pot apărea variații între aceste două stări din cauza modificărilor pH-ului, temperaturii și compoziției soluției. În stare dizolvată, cobaltul se găsește sub formă de complexe organice. Râurile și lacurile au caracteristica că cobaltul este reprezentat de un cation divalent. În prezența un numar mare oxidanți în soluție, cobaltul poate fi oxidat la un cation trivalent.
Face parte din plante și animale, pentru că se joacă rol importantîn dezvoltarea lor. Este unul dintre principalele oligoelemente. Dacă există o deficiență de cobalt în sol, atunci nivelul acestuia în plante va fi mai mic decât de obicei și, ca urmare, pot apărea probleme de sănătate la animale (există riscul de anemie). Acest fapt se observă mai ales în zona non-cernoziom de taiga-pădure. Face parte din B 12, reglează absorbția substanțelor azotate, crește nivelul de clorofilă și acid ascorbic. Fără el, plantele nu pot crește suma necesară veveriţă. Ca toate metalele grele, poate fi toxic cantitati mari.
Conținutul de cobalt din apele naturale
- Nivelurile de cobalt din râuri variază de la câteva micrograme la miligrame pe litru.
- În mări, nivelul mediu de cadmiu este de 0,5 µg/l.
Concentrația maximă admisă de cobalt pentru mediul acvatic
MPC pentru cobalt pentru mediul acvatic este de 0,1 mg/l, iar în iazurile piscicole, MPC pentru fermele piscicole este de 0,01 mg/l.
Mangan (Mn)
Manganul intră în râuri și lacuri prin aceleași mecanisme ca și fierul. În principal, eliberarea acestui element în soluție are loc în timpul leșierii mineralelor și minereurilor care conțin mangan (ocru negru, brownit, piroluzit, psilomelan). Manganul poate proveni și din descompunerea diferitelor organisme. Industria are, cred, cel mai mare rol în poluarea cu mangan (apele reziduale din mine, industria chimica, metalurgie).
Scăderea cantității de metal asimilabil în soluție are loc, ca și în cazul altor metale în condiții aerobe. Mn(II) este oxidat la Mn(IV), drept urmare precipită sub formă de MnO2. Factori importanțiîn astfel de procese se iau în considerare temperatura, cantitatea de oxigen dizolvat în soluție și pH-ul. O scădere a manganului dizolvat în soluție poate apărea atunci când este consumat de alge.
Manganul migrează în principal sub formă de suspensii, care, de regulă, indică compoziția rocilor din jur. Îl conțin în amestec cu alte metale sub formă de hidroxizi. Predominanța manganului în formă coloidală și dizolvată indică faptul că acesta este asociat cu compusi organici formând complexe. Complexele stabile se văd cu sulfați și bicarbonați. Cu clorul, manganul formează complexe mai rar. Spre deosebire de alte metale, este mai slab reținut în complexe. Manganul trivalent formează astfel de compuși numai în prezența liganzilor agresivi. Alte forme ionice (Mn 4+ , Mn 7+) sunt mai puțin rare sau nu se găsesc deloc în condiții normale în râuri și lacuri.
Conținutul de mangan în corpurile naturale de apă
Mările sunt considerate cele mai sărace în mangan - 2 μg / l, în râuri conținutul său este mai mare - până la 160 μg / l, dar rezervoarele subterane sunt deținătoare de recorduri de această dată - de la 100 μg la câțiva mg / l.
Manganul se caracterizează prin fluctuații sezoniere ale concentrației, precum fierul.
Au fost identificați mulți factori care afectează nivelul de mangan liber în soluție: legătura râurilor și lacurilor cu rezervoarele subterane, prezența organismelor fotosintetice, conditii aerobe, descompunerea biomasei (organisme și plante moarte).
Un rol biochimic important al acestui element, deoarece este inclus în grupul de microelemente. Multe procese sunt inhibate în deficiența de mangan. Crește intensitatea fotosintezei, participă la metabolismul azotului, protejează celulele de impact negativ Fe(II) în timp ce îl oxidează la forma trivalentă.
Concentrația maximă admisă de mangan pentru mediul acvatic
MPC pentru mangan pentru rezervoare - 0,1 mg/l.
Cupru (Cu)
Nici un singur microelement nu are un rol atât de important pentru organismele vii! Cuprul este unul dintre cele mai căutate oligoelemente. Face parte din multe enzime. Fără el, aproape nimic nu funcționează într-un organism viu: sinteza proteinelor, vitaminelor și este perturbată. Fără el, plantele nu se pot reproduce. Cu toate acestea, o cantitate în exces de cupru provoacă o mare intoxicație în toate tipurile de organisme vii.
Nivelurile de cupru în apele naturale
Deși cuprul are două forme ionice, Cu(II) apare cel mai frecvent în soluție. De obicei, compușii Cu(I) sunt greu solubili în soluție (Cu2S, CuCl, Cu2O). Cupru acvaionic diferiți pot apărea în prezența oricăror liganzi.
Cu utilizarea mare de astăzi a cuprului în industrie și Agricultură, acest metal poate provoca poluarea mediului. Combinațiile chimice, uzinele metalurgice, minele pot fi surse de ape uzate cu conținut ridicat de cupru. Procesele de eroziune ale conductelor contribuie, de asemenea, la contaminarea cu cupru. Cele mai importante minerale cu un continut ridicat de cupru sunt malachitul, bornitul, calcopirita, calcocitul, azurita, brontantina.
Concentrația maximă admisă de cupru pentru mediul acvatic
MPC-ul cuprului pentru mediul acvatic este considerat a fi de 0,1 mg/l; în iazurile piscicole, MPC-ul fermei piscicole a cuprului este redus la 0,001 mg/l.
Molibden (Mo)
În timpul leșierii mineralelor cu un conținut ridicat de molibden, conexiuni diferite molibden. Nivel inalt molibdenul poate fi văzut în râurile și lacurile care sunt aproape de fabricile de valorificare și întreprinderile de metalurgie neferoasă. Datorită diferitelor procese de precipitare a compușilor puțin solubili, adsorbția la suprafață diferite rase, precum și utilizarea de alge și plante acvatice, cantitatea acesteia poate scădea semnificativ.
În cea mai mare parte în soluție, molibdenul poate fi sub formă de anion MoO 4 2-. Există posibilitatea prezenței complexelor molibden-organice. Datorită faptului că în timpul oxidării molibdenitei se formează compuși liberi fin dispersați, nivelul de molibden coloidal crește.
Conținutul de molibden în rezervoare naturale
Nivelurile de molibden din râuri variază între 2,1 și 10,6 µg/l. În mări și oceane, conținutul său este de 10 mcg / l.
La concentrații mici, molibdenul ajută la dezvoltarea normală a organismului (atât vegetal, cât și animal), deoarece este inclus în categoria microelementelor. De asemenea, el este parte integrantă diverse enzime, cum ar fi xantin-oxilaza. Cu o lipsă de molibden, apare o deficiență a acestei enzime și astfel pot apărea efecte negative. Nici un exces din acest element nu este binevenit, deoarece metabolismul normal este perturbat.
Concentrația maximă admisă de molibden pentru mediul acvatic
MPC pentru molibden din corpurile de apă de suprafață nu trebuie să depășească 0,25 mg/l.
Arsenic (As)
Contaminate cu arsenic sunt în principal zonele care se află în apropierea minelor de minerale cu un conținut ridicat de acest element (wolfram, cupru-cobalt, minereuri polimetalice). O cantitate foarte mică de arsenic poate apărea în timpul descompunerii organismelor vii. Datorită organismelor acvatice, acesta poate fi absorbit de acestea. Asimilarea intensivă a arsenului din soluție se observă în perioada de dezvoltare rapidă a planctonului.
Cei mai importanți poluanți cu arsenic sunt considerați a fi industria de îmbogățire, întreprinderile de producere a coloranților, precum și agricultura.
Lacurile și râurile conțin arsen în două stări: suspendat și dizolvat. Proporțiile dintre aceste forme pot varia în funcție de pH-ul soluției și de compoziția chimică a soluției. În stare dizolvată, arsenul poate fi trivalent sau pentavalent, intrând în forme anionice.
Nivelurile de arsen din apele naturale
În râuri, de regulă, conținutul de arsenic este foarte scăzut (la nivelul de µg/l), iar în mări - o medie de 3 µg/l. niste apă minerală poate conține cantități mari de arsenic (până la câteva miligrame pe litru).
Majoritatea arsenului poate conține rezervoare subterane - până la câteva zeci de miligrame pe litru.
Compușii săi sunt foarte toxici pentru toate animalele și pentru oameni. În cantități mari, procesele de oxidare și transportul oxigenului către celule sunt perturbate.
Concentrația maximă admisă de arsenic pentru mediul acvatic
MPC pentru arsen pentru mediul acvatic este de 50 µg/l, iar în iazurile de pescuit, MPC pentru fermele piscicole este de asemenea de 50 µg/l.
Nichel (Ni)
Conținutul de nichel din lacuri și râuri este influențat de rocile locale. Dacă în apropierea rezervorului există depozite de minereuri de nichel și fier-nichel, concentrația poate fi chiar mai mare decât în mod normal. Nichelul poate pătrunde în lacuri și râuri atunci când plantele și animalele se descompun. Algele albastre-verzi conțin cantități record de nichel în comparație cu alte organisme vegetale. Apele uzate importante cu un conținut ridicat de nichel sunt degajate în timpul producției de cauciuc sintetic, în timpul proceselor de nichelare. De asemenea, nichelul este eliberat în cantități mari în timpul arderii cărbunelui și petrolului.
pH-ul ridicat poate determina precipitarea nichelului sub formă de sulfați, cianuri, carbonați sau hidroxizi. Organismele vii pot reduce nivelul de nichel mobil prin consumul acestuia. Procesele de adsorbție pe suprafața rocii sunt de asemenea importante.
Apa poate conține nichel în forme dizolvate, coloidale și în suspensie (echilibrul dintre aceste stări depinde de pH-ul mediului, temperatură și compoziția apei). Hidroxidul de fier, carbonatul de calciu, argila absorb bine compușii care conțin nichel. Nichelul dizolvat este sub formă de complexe cu acizi fulvici și humici, precum și cu aminoacizi și cianuri. Ni 2+ este considerată cea mai stabilă formă ionică. Ni 3+ se formează de obicei la pH ridicat.
La mijlocul anilor 1950, nichelul a fost adăugat pe lista oligoelementelor deoarece joacă un rol important în diferite procese ca catalizator. În doze mici, are un efect pozitiv asupra proceselor hematopoietice. Dozele mari sunt încă foarte periculoase pentru sănătate, deoarece nichelul este un element chimic cancerigen și poate provoca diferite boli ale sistemului respirator. Ni 2+ liber este mai toxic decât sub formă de complexe (de aproximativ 2 ori).
Nivelul de nichel în apele naturale
Concentrația maximă admisă de nichel pentru mediul acvatic
MPC pentru nichel pentru mediul acvatic este de 0,1 mg/l, dar în iazurile de pescuit, MPC pentru fermele piscicole este de 0,01 mg/l.
staniu (Sn)
Sursele naturale de staniu sunt mineralele care conțin acest element (stanin, casiterit). Sursele antropogenice sunt fabricile și fabricile pentru producerea diverselor vopsele organice și industria metalurgică care lucrează cu adaos de cositor.
Staniul este un metal cu toxicitate scăzută, motiv pentru care mâncând din metal conservat nu ne riscăm sănătatea.
Lacurile și râurile conțin mai puțin de un microgram de staniu pe litru de apă. Rezervoarele subterane pot conține câteva micrograme de staniu pe litru.
Concentrația maximă admisă de staniu pentru mediul acvatic
MPC de staniu pentru mediul acvatic - 2 mg/l.
Mercur (Hg)
În principal, nivel ridicat mercurul în apă este văzut în zonele în care există depozite de mercur. Cele mai comune minerale sunt livingstone, cinabru, metacinabarit. Apele uzate din fabricile farmaceutice, de pesticide și de coloranți pot conține cantități importante de mercur. O altă sursă importantă de poluare cu mercur este centrale termice(care folosesc cărbunele drept combustibil).
Nivelul său în soluție scade în principal din cauza animalelor și plantelor marine, care acumulează și chiar concentrează mercur! Uneori, conținutul de mercur în viața marină crește de câteva ori mai mult decât în mediul marin.
Apa naturală conține mercur în două forme: în suspensie (sub formă de compuși absorbiți) și dizolvat (compuși complexi, minerali ai mercurului). În anumite zone ale oceanelor, mercurul poate apărea ca complexe de metilmercur.
Mercurul și compușii săi sunt foarte toxici. La concentrații mari, are un efect negativ asupra sistem nervos, provoacă modificări în sânge, afectează secreția tractului digestiv și funcția motorie. Produsele prelucrării mercurului de către bacterii sunt foarte periculoase. Ei pot sintetiza substanțe organice pe bază de mercur, care sunt de multe ori mai toxice decât compușii anorganici. Când consumăm pește, compușii de mercur pot pătrunde în corpul nostru.
Concentrația maximă admisă de mercur pentru mediul acvatic
MPC de mercur în apă obișnuită- 0,5 µg/l, iar în iazurile piscicole MPC pentru fermele piscicole este mai mică de 0,1 µg/l.
Plumb (Pb)
Râurile și lacurile pot fi poluate cu plumb în mod natural atunci când mineralele de plumb sunt spălate (galena, anglesite, cerusită) și într-un mod antropic (arderea cărbunelui, utilizarea plumbului tetraetil în combustibil, deversările din fabricile de prelucrare a minereurilor, ape uzate din mine şi uzine metalurgice). Precipitarea compușilor de plumb și adsorbția acestor substanțe pe suprafața diferitelor roci sunt cele mai importante metode naturale de scădere a nivelului acestuia în soluție. Dintre factorii biologici, hidrobionții conduc la o scădere a nivelului de plumb în soluție.
Plumbul din râuri și lacuri este în formă suspendată și dizolvată (complexe minerale și organo-minerale). De asemenea, plumbul este sub formă de substanțe insolubile: sulfați, carbonați, sulfuri.
Conținut de plumb în apele naturale
Am auzit multe despre toxicitatea acestui metal greu. Este foarte periculos chiar și în cantități mici și poate provoca intoxicație. Plumbul intră în organism prin sistemele respirator și digestiv. Excreția sa din organism este foarte lentă și se poate acumula în rinichi, oase și ficat.
Concentrația maximă admisă de plumb pentru mediul acvatic
MPC-ul plumbului pentru mediul acvatic este de 0,03 mg/l, iar în iazurile piscicole, MPC-ul fermelor piscicole este de 0,1 mg/l.
Tetraetil plumb
Acesta servește ca agent antidetonant în carburanții pentru motoare. Astfel, principalele surse de poluare cu această substanță sunt vehiculele.
Acest compus este foarte toxic și se poate acumula în organism.
Concentrația maximă admisă de tetraetil plumb pentru mediul acvaticNivelul maxim admis al acestei substanțe se apropie de zero.
În general, plumbul tetraetil nu este permis în compoziția apelor.
Argint (AG)
Argintul pătrunde în principal în râuri și lacuri din rezervoarele subterane și ca urmare a deversării apelor uzate din întreprinderi (întreprinderi fotografice, fabrici de îmbogățire) și mine. O altă sursă de argint poate fi agenții algicizi și bactericizi.
În soluție, cei mai importanți compuși sunt sărurile cu halogenură de argint.
Conținut de argint în apele naturale
În râurile și lacurile curate, conținutul de argint este mai mic de un microgram pe litru, în mări - 0,3 µg/l. Rezervoarele subterane conțin până la câteva zeci de micrograme pe litru.
Argintul sub formă ionică (la anumite concentrații) are efect bacteriostatic și bactericid. Pentru a putea steriliza apa cu argint, concentrația acesteia trebuie să fie mai mare de 2 * 10 -11 mol / l. Rolul biologic argintul din corp nu este încă bine cunoscut.
Concentrația maximă admisă de argint pentru mediul acvatic
Argint maxim admisibil pentru mediul acvatic este de 0,05 mg/l.
PEEP - concentrația maximă admisă a unei substanțe în apa unui rezervor pentru consumul de apă potabilă și menajeră, mg / l. Această concentrație nu trebuie să aibă un efect direct sau indirect asupra corpului uman de-a lungul vieții, precum și asupra sănătății generațiilor următoare și nu ar trebui să înrăutățească condițiile de igienă pentru utilizarea apei. PEEP.r. - Concentrația maximă admisă a unei substanțe în apa unui rezervor utilizat în scopuri piscicole, mg/l.
Evaluarea calității ecosistemelor acvatice se bazează pe documente normative și directive care utilizează evaluări hidrogeochimice directe. În tabel. 2.4, de exemplu, sunt date criteriile de evaluare a poluării chimice a apelor de suprafață.
Sunt stabilite limite pentru apă concentrații admisibile peste 960 compuși chimici, care se combină în trei grupe după următorii indicatori limitatori de nocivitate (LPV): sanitar-toxicologici (s.-t.); sanitare generale (gen.); organoleptic (org.).
MPC a unor substanțe nocive în mediu acvatic sunt prezentate în tabel. 2.1.4.
Cel mai cerințe ridicate aplicat pe apa potabila. Standard de stat pe apa folosita pentru baut si Industria alimentară(SanPiN 2.1.4.1074-01), determină indicatorii organoleptici ai apei care sunt favorabili omului: gust, miros, culoare, transparență, precum și inofensivitatea compoziției sale chimice și siguranța epidemiologică.
Tabelul 2.1.4
MPC de substanțe nocive în corpurile de apă de uz casnic și potabil
utilizare culturală și menajeră a apei, mg/l
(GN 2.1.5.689-98)
| Substanțe | LPV | MPC |
| 1 | 2 | 3 |
| />Bor | Sf. | 0,5 |
| Brom | Sf. | 0,2 |
| Bismut | Sf. | 0,1 |
| Hexaclorbenzen | Sf. | 0,05 |
| Dimetilamină | Sf. | 0,1 |
| Difluordiclormetan (freon) | Sf. | 10 |
| dietil eter | Org. | 0,3 |
| Fier | Org. | 0,3 |
| Izopren | Org. | 0,005 |
| Cadmiu | Sf. | 0,001 |
| Karbofos | Org. | 0,05 |
| Kerosen: | | |
| oxidat | Org. | 0,01 |
| Iluminat (GOST 4753-68) | Org. | 0,05 |
| Tehnic | Org. | 0,001 |
| Acid: | | |
| benzoic | Tot. | 0,6 |
| Difenilacetic | Tot. | 0,5 |
| uleios | Tot. | 0,7 |
| Formic | Tot. | 3,5 |
| Acetic | Tot. | 1,2 |
| Acizi grași sintetici | Tot. | 0,1 |
| C5-C20 | | |
| Mangan | Org. | 0,1 |
| Cupru | Org. | 1 |
| metanol | Sf. | 3 |
| Molibden | Sf. | 0,25 |
| Uree | Tot. | 1 |
| Naftalină | Org. | 0,01 |
| Ulei: | | |
| polisulfuroase | Org. | 0,1 |
| durabil | Org. | 0,3 |
| Nitrați pentru: | | |
| NUMARUL 3- | Sf. | 45 |
| NO2- | Sf. | 3,3 |
| Polietilenamină | Sf. | 0,1 |
| Tiocianați | Sf. | 0,1 |
| Mercur | Sf. | 0,0005 |
| Conduce | Sf. | 0,03 |
| disulfură de carbon | Org. | 1 |
| Terebentină | Org. | 0,2 |
| sulfuri | Tot. | Absența |
| Tetraetil plumb | Sf. | Absența |
| Tributil Fosfat | Tot. | 0,01 |
Apa de băut în orice moment al anului nu trebuie să conțină mai puțin de 4 g/m de oxigen, iar prezența impurităților minerale (mg/l) în ea nu trebuie să depășească: sulfați (SO4 -) - 500; cloruri (Cl -) - 350; fier (Fe2+ + Fe3+) - 0,3; mangan (Mn2+) - 0,1; cupru (Cu2+) - 1,0; zinc (Zn2+) - 5,0; aluminiu (Al) - 0,5; metafosfați (PO3 ") - 3,5; fosfați (PO4
3") - 3,5; reziduu uscat - 1000. Astfel, apa este potrivită pentru băut dacă mineralizarea sa totală nu depășește 1000 mg / l. Mineralizarea foarte scăzută a apei (sub 1000 mg / l) îi înrăutățește și gustul, iar apa , în general lipsit de săruri (distilat), este dăunător sănătății, deoarece utilizarea sa perturbă digestia și activitatea glandelor endocrine. Uneori, în acord cu organele serviciului sanitar și epidemiologic, un conținut de reziduuri uscate de până la 1500 mg/l este permis.
Indicatori care caracterizează poluarea lacurilor de acumulare și a apei potabile cu substanțe clasificate în clasele de pericol 3 și 4, precum și proprietăți fizico-chimice iar caracteristicile organoleptice ale apei sunt suplimentare. Acestea sunt utilizate pentru a confirma gradul de intensitate al poluării antropice a surselor de apă, stabilit prin indicatori prioritari.
Aplicarea diferitelor criterii de evaluare a calității apei ar trebui să se bazeze pe avantajul cerințelor de utilizare a apei ale cărei criterii sunt mai stricte. De exemplu, dacă un corp de apă este utilizat simultan în scopuri de băut și de pescuit, atunci pot fi impuse cerințe mai stricte (de mediu și pescuit) privind evaluarea calității apei.
PCP-10 (indicator al poluării chimice). Acest indicator este deosebit de important pentru zonele în care se observă poluare chimică pentru mai multe substanțe simultan, fiecare dintre acestea depășind de multe ori MPC. Se calculează numai la identificarea zonelor de urgență ecologică și a zonelor de dezastru ecologic.
Calculul se efectuează pentru zece compuși care depășesc maxim MPC, conform formulei:
PKhZ-10 = C1 / MPC1 + C2 / MPC2 + C3 / MPC3 + ... C10 / MPC10,
unde Cb C2, C3 ... Cb - concentrația de substanțe chimice în apă: MPC - pescuit.
Când se determină PCP-10 pentru substanțele chimice pentru care nu există o valoare relativ satisfăcătoare a poluării apei, raportul C/MAC este considerat condiționat egal cu 1.
Pentru stabilirea PCP-10, se recomandă analizarea apei în funcție de numărul maxim posibil de indicatori.
Indicatorii suplimentari includ fizico-chimici general acceptați și caracteristici biologice dând ideea generala asupra compoziției și calității apei. Acești indicatori sunt utilizați pentru a caracteriza suplimentar procesele care au loc în corpurile de apă. În plus, în caracteristici suplimentare includ indicatori care iau în considerare capacitatea poluanților de a se acumula în sedimentele de fund și hidrobionți.
Coeficientul de acumulare inferioară a CDA este calculat prin formula:
KDA \u003d Sd.o. / Sv,
unde Sd. despre. și Sv - concentrația de poluanți în sedimentele de fund și, respectiv, în apă.
Coeficientul de acumulare în hidrobionți:
Kn \u003d Sg / Sv,
unde Cr este concentrația de poluanți din hidrobionți.
Concentrațiile critice de substanțe chimice (CC) sunt determinate conform metodologiei de determinare a concentrațiilor critice de poluanți elaborată de Comitetul de Stat pentru Hidrometeorologie în 1983.
Valorile medii CC ale unor poluanți sunt, mg/l: cupru - 0,001 ... 0,003; cadmiu - 0,008 ... 0,020; zinc - 0,05...0,10; PCB - 0,005; benzo(a)piren - 0,005.
Atunci când se evaluează starea ecosistemelor acvatice, indicatorii suficient de fiabili sunt caracteristicile stării și dezvoltării tuturor grupuri de mediu comunitate de apă.
La identificarea zonelor luate în considerare, indicatorii sunt utilizați pentru bacterio-, fito- și zooplancton, precum și pentru ihtiofaună. În plus, pentru a determina gradul de toxicitate al apelor, se utilizează un indicator integral - biotestare (pentru crustacee inferioare). În acest caz, toxicitatea corespunzătoare a masei de apă trebuie observată în toate fazele principale ale ciclului hidrologic.
Principalii indicatori pentru fito- și zooplancton, precum și pentru zoobentos, au fost luați pe baza datelor de la serviciile regionale de control hidrobiologic care caracterizează gradul de degradare ecologică a ecosistemelor de apă dulce.
Parametrii indicatorilor propuși pentru alocarea zonelor pe un anumit teritoriu ar trebui să fie formați pe baza unor observații suficient de lungi (cel puțin trei ani).
Trebuie avut în vedere faptul că valorile indicatoare ale speciilor pot fi diferite în diferite zonele climatice.
Atunci când se evaluează starea ecosistemelor acvatice, indicatorii ihtiofaunei sunt importanți, în special pentru corpurile de apă și rezervoarele unice, special protejate, din prima și cea mai înaltă categorie de pescuit.
DBO - cerere biologică de oxigen - cantitatea de oxigen utilizată în procesele biochimice de oxidare a substanțelor organice (cu excepția proceselor de nitrificare) pentru un anumit timp de incubare a probei (2, 5, 20, 120 de zile), mg O2 / l de apă ( BODp - timp de 20 de zile, BOD5 - timp de 5 zile).
Procesul oxidativ în aceste condiții este realizat de microorganisme care folosesc componente organice ca hrană. Metoda BOD este următoarea. După o decantare de două ore, apa uzată investigată se diluează cu apă curată, luată în asemenea cantitate încât oxigenul conținut în ea să fie suficient pentru a oxida complet toate substanțele organice din apa reziduală. După ce s-a determinat conținutul de oxigen dizolvat în amestecul rezultat, acesta este lăsat într-o sticlă închisă timp de 2, 3, 5, 10, 15 zile, determinându-se conținutul de oxigen după fiecare dintre perioadele de timp enumerate (perioada de incubație). Scăderea cantității de oxigen din apă arată cât de mult a fost cheltuită în acest timp pentru oxidarea substanțelor organice din apele uzate. Această cantitate, raportată la 1 litru de apă uzată, este un indicator al consumului biochimic de oxigen de către apa uzată pentru o anumită perioadă de timp (BOD2, BODz, BOD5, BODy, BOD15).
Trebuie remarcat faptul că consumul de oxigen biochimic nu include consumul acestuia pentru nitrificare. Prin urmare, trebuie efectuată o DBO completă înainte de începerea nitrificării, care de obicei începe după 15-20 de zile. DBO al apei uzate se calculează folosind formula:
BOD = [(a1 ~ b1) ~ (a2 ~ b2)] X 1000
V'
unde ai este concentrația de oxigen din proba pregătită pentru determinare la începutul incubației (în „ziua zero”), mg/l; а2 - concentrația de oxigen în apa de diluare la începutul incubației, mg/l; b1 - concentrația de oxigen în probă la sfârșitul incubației, mg/l; b2 este concentrația de oxigen din apa de diluție la sfârșitul incubației, mg/l; V este volumul de apă uzată conținut în 1 litru de probă, după toate diluțiile, ml.
COD - nevoie chimicăîn oxigen, determinată prin metoda bicromatului, i.e. cantitatea de oxigen echivalentă cu cantitatea de oxidant consumat necesară pentru oxidarea tuturor agenților reducători conținuti în apă, mg O2/l apă.
Consumul chimic de oxigen, exprimat ca număr de miligrame de oxigen per 1 litru de apă uzată, se calculează prin formula:
HPC - 8(a - b)x N1000
V'
unde a este volumul de soluție de sare Mohr utilizată pentru titrare într-un experiment martor, ml; b este volumul aceleiași soluții utilizate pentru titrarea probei, ml; N este normalitatea soluției titrate de sare Mohr; V este volumul de apă uzată analizată, ml; 8 - echivalent oxigen.
În raport cu BODp/COD, se apreciază eficiența oxidării biochimice a substanțelor.
